Zieveho syndrom
Libuše Husová Orcid.org 1, Jan Trna Orcid.org 2, Milan Dastych Jr.3, Leoš Křen Orcid.org
+ Pracoviště
Souhrn
Autoři popisují případ 33letého muže se Zieveho syndromem, který vznikl v závislosti na vysokém příjmu alkoholu. Pacient byl přijat k hospitalizaci pro bolesti břicha, nechutenství a žloutenku. Při přijetí byl diagnostikován subileózní stav a rozvoj poruchy vědomí - somnolence. V laboratorních testech byla zjištěna hyperbilirubinémie, hemolytická anémie, extrémní hyperlipidémie a zvýšené hodnoty aminotransferáz. Computerová tomografie prokázala hepatomegalii bez ložiskových změn, jaterní biopsie diagnostikovala steatohepatitidu až steatofibrózu. Po konzervativní terapii spočívající v adekvátním nutričním příjmu živin a suplementaci vitaminů a stopových prvků parenterálně a následně v kombinaci s dietou s omezením tuků došlo k postupné úpravě klinického stavu i laboratorních hodnot.
Klíčová slova: hemolytická anémie - hyperlipidémie - Zieveho syndrom - žloutenka.
ÚVOD
Triádu žloutenky, hyperlipidémie a tranzitorní hemolytické anémie poprvé popsal Leslie Zieve v roce 1957 u 20 mužů (průměrného věku 39 let) s anamnézou chronického alkoholizmu. U tohoto syndromu se mohou vyskytnout v klinickém obraze subfebrílie a bolest břicha(1). Syndrom je často provázen laboratorními známkami cholestázy Příčinou hemolýzy je poškození membrány erytrocytů. Většinou dochází k jejich tvarovým abnormalitám (akantocyty poikilocyty stomatocyty) s nálezem vakuolizovaných erytroblastů v kostní dřeni. Příčina těchto změn není jasná. Uvažuje se o možném toxickém účinku žlučových kyselin nebo proteolytických enzymů(2). Metabolizmus červených krvinek je u těchto nemocných abnormální, predisponující k hemolýze, a to pravděpodobně v důsledku zvýšených hladin cirkulujícího hemolyzinu a lyzolecitinu, které byly u těchto nemocných prokázány. Hyperlipidémie často předchází epizodu hemolýzy(3,4). Tento syndrom obvykle provází akutní alkoholickou hepatitidu bez přechodu do cirhózy(5). V histologickém obrazu je přítomna velkokapénková steatóza nebo steatohepatitida s cholestázou.
Prognóza je většinou dobrá, nicméně může mít i fulminantní průběh(2). Není známá specifická terapie, taje stejná jako u akutní alkoholické hepatitidy a někdy je pro výraznou anemii nutná krevní transfuze(6,7). Kortikosteroidy se považují v léčbě Zieveho syndromu za nevhodné(1).
POPIS PŘÍPADU
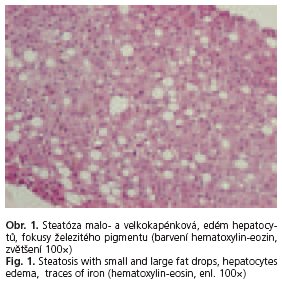
Třicetitříletý pacient byl přivezen rychlou záchranou službou na chirurgickou ambulanci pro bolesti břicha, nauzeu a zvracení s postupně se rozvíjející poruchou vědomí (somnolence). V minulosti byl pacient vyšetřován pro hepatopatii nejasné etiologie s cholestatickými rysy (zvýšené hodnoty bilirubinu a gamaglutamyltransferázy), opakovaně však odmítl došetření onemocnění. V předchorobí byl léčen pro vředovou chorobu duodena. Trvale neužíval žádné léky. Při přijetí udával váhový úbytek asi 10 kg pro opakované bolesti břicha za půlroční období, stran pravidelného příjmu alkoholu přiznával 1 pivo lx týdně, destiláty a víno zcela negoval. Při přijetí na naše pracoviště byl pacient nesoustředěný ale spolupracující a orientovaný časem a místem, v popředí klinického obrazu byl výrazný ikterus kůže, obleněná peristaltika břicha, hepatomegalie + 6 cm. Na prostém snímku břicha ve stoje byly v oblasti středního mezo-hypogastria a pravého hypogastria dilatované kličky tenkého střeva na 4,5 cm a ojedinělé hladinky v této oblasti. Z laboratorních hodnot byla výrazná elevace celkového bilirubinu (bili) 93 μmol/1, s převahou nekonjugovaného bili oproti přímému bili 29,4 μmol/1, elevace alaninaminotransferázy (ALT) 3,82 μkat/1, asparátamino-transferázy (AST) 10,37 μkat/1, gama-glutamyl-transferázy (GMT) 89,32 μkat/1 a alkalické fosfatázy (ALP) 13,96 μkat/1. U pacienta byly tedy v laboratoři nalezeny převažující známky cholestatického ikteru s extrémní hodnotou GMT. Dále byla diagnostikována výrazná porucha lipidového metabolizmu, která byla provázena mléčně zkaleným sérem: cholestrol (chol) 26,8 mmol/1, triglyceridy (TG) 36,29 mmol/l. U nemocného byla také lehce snížená hodnota celkové bílkoviny (CB) 63,4 g/l a albuminu 32,3 g/l. V krevním obrazu byla zjištěna anémie, trombocytopenie a retikulocytóza: erytrocyty 3,47 x 109/l, hemoglobin 119 g/l, střední objem erytrocytů (MCV) 91,1 fl, trombocyty 123 109/1 a retikulocyty 5,8 %. Hodnoty sérového železa byly v mezích normy 24,3 μmol/1, hodnoty feritinu byly značně zvýšeny nad 2000 μg/1, stejně jako hodnoty volného hemoglobinu 305 mg/l. 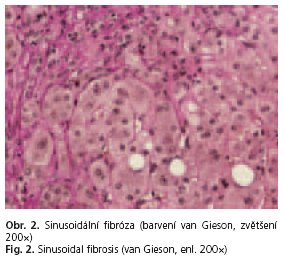 Diferenciálně diagnostická vyšetření objasňující etiologii jaterní choroby byla negativní (virové hepatitidy, autoimunní hepatitidy, Wilsonova choroba, porfyrie, hemochromatóza atd.). Byla avšak zjištěna vyšší hladina karbohydrát-deficientního transferinu (CDT) 6,4 % a pacient byl znovu podroben anamnéze, kdy se již nezdráhal přiznat pravidelný příjem alkoholu. V posledním půlroce pil větší množství piva nejméně 3-9 piv denně, příjem alkoholu byl nuceně snížen (ne však vyloučen) poslední měsíc pro bolesti břicha a pocit nevolnosti, společně s příjmem alkoholu byl snížen i příjem stravy, a to ze stejných důvodů. Provedené ultrazvukové vyšetření prokázalo játra difuzně zvětšená, zvýšeně echogenní, bez přesvědčivých ložiskových změn a bez dilatace žlučových cest. Žlučník však s difuzně zesílenou stěnou až kolem 1 cm, bez prokázané litiázy Nález byl uzavřen jako cholecystitis s výrazně prosáklou stěnou a difuzní hepatopatii. Bylo provedeno vyšetření computerovou tomografií (CT) s potvrzením hepatomegalie s difuzní hepatopatii, žlučník v CT obraze prostorný, bez patologického sycení stěny, tedy v CT obrazu bez prokázané patologie. Gastrofibroskopické vyšetření vyloučilo onemocnění jícnu, žaludku a duodena. Provedená jaterní biopsie prokázala zachovanou lalůčkovitou jaterní architektoniku s přítomností lobulární aktivity s neutrofilní reakcí (skóre dle Ishaka 2), centroacinózní steatózou převážně velkokapénkovou, mírnou depozici železa v hepatocytech a periportální, sinusoidální a perivenulární fibrózu (skóre 4-5 dle Ishaka). Nález odpovídal toxonutritivní statohepatitidě/steatofibróze dle Ishaka 3-4 (obr. 1 a 2). Na základě žloutenky, hemolytické anémie, hyperlipidémie, bolestí břicha a alkoholické steatohepatitidy byla stanovena diagnóza Zieveho syndromu. U pacienta byla zavedena beztuková parenterální výživa a následně dieta s omezením tuků.
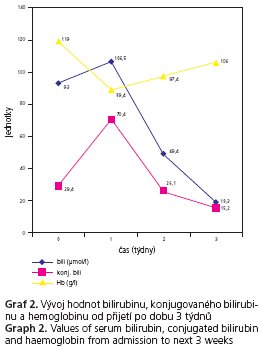
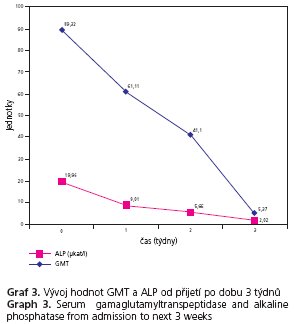
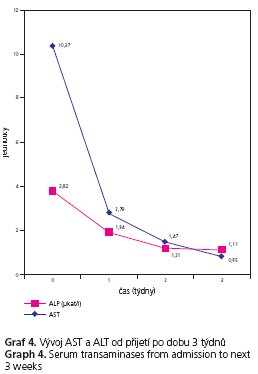
Diferenciálně diagnostická vyšetření objasňující etiologii jaterní choroby byla negativní (virové hepatitidy, autoimunní hepatitidy, Wilsonova choroba, porfyrie, hemochromatóza atd.). Byla avšak zjištěna vyšší hladina karbohydrát-deficientního transferinu (CDT) 6,4 % a pacient byl znovu podroben anamnéze, kdy se již nezdráhal přiznat pravidelný příjem alkoholu. V posledním půlroce pil větší množství piva nejméně 3-9 piv denně, příjem alkoholu byl nuceně snížen (ne však vyloučen) poslední měsíc pro bolesti břicha a pocit nevolnosti, společně s příjmem alkoholu byl snížen i příjem stravy, a to ze stejných důvodů. Provedené ultrazvukové vyšetření prokázalo játra difuzně zvětšená, zvýšeně echogenní, bez přesvědčivých ložiskových změn a bez dilatace žlučových cest. Žlučník však s difuzně zesílenou stěnou až kolem 1 cm, bez prokázané litiázy Nález byl uzavřen jako cholecystitis s výrazně prosáklou stěnou a difuzní hepatopatii. Bylo provedeno vyšetření computerovou tomografií (CT) s potvrzením hepatomegalie s difuzní hepatopatii, žlučník v CT obraze prostorný, bez patologického sycení stěny, tedy v CT obrazu bez prokázané patologie. Gastrofibroskopické vyšetření vyloučilo onemocnění jícnu, žaludku a duodena. Provedená jaterní biopsie prokázala zachovanou lalůčkovitou jaterní architektoniku s přítomností lobulární aktivity s neutrofilní reakcí (skóre dle Ishaka 2), centroacinózní steatózou převážně velkokapénkovou, mírnou depozici železa v hepatocytech a periportální, sinusoidální a perivenulární fibrózu (skóre 4-5 dle Ishaka). Nález odpovídal toxonutritivní statohepatitidě/steatofibróze dle Ishaka 3-4 (obr. 1 a 2). Na základě žloutenky, hemolytické anémie, hyperlipidémie, bolestí břicha a alkoholické steatohepatitidy byla stanovena diagnóza Zieveho syndromu. U pacienta byla zavedena beztuková parenterální výživa a následně dieta s omezením tuků. 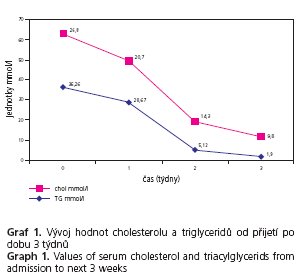 Důraz byl kladen na dostatečný příjem vitaminů a stopových prvků parenterální a dále enterální cestou. Postupně došlo k úpravě klinického stavu, pacient byl bez subjektivních potíží. Během hospitalizace se postupně upravovaly i laboratorní výsledky. Normálních hodnot dosáhly koncentrace bili 19,3 umol/l, konjugovaného bili 15,2 μmol/l, AST 0,85 μkat/l, ALP 2,02 μkat/l a TG 1,9 mmo/l. Výrazně poklesla i hodnota celkového cholesterolu na 9,8 mmol/l a GMT na 5,37 μkat/l, téměř normě se blížila hodnota ALT 1,11 ukat/l. Po výrazném poklesu hemoglobinu (89,4 g/l) při akutní hemolytické anémii došlo k pozvolnému zvýšení těchto hodnot (106 g/l) v průběhu 2. a 3. týdne terapie bez nutnosti podání krevní transfuze. Vývoj laboratorních hodnot v časovém horizontu od přijetí po dobu 3 týdnů (chol, TG, bili, kojugovaného bili, AST, ALT, GMT, ALP, a Hb) je dokumentován v grafech 1 až 4.
Důraz byl kladen na dostatečný příjem vitaminů a stopových prvků parenterální a dále enterální cestou. Postupně došlo k úpravě klinického stavu, pacient byl bez subjektivních potíží. Během hospitalizace se postupně upravovaly i laboratorní výsledky. Normálních hodnot dosáhly koncentrace bili 19,3 umol/l, konjugovaného bili 15,2 μmol/l, AST 0,85 μkat/l, ALP 2,02 μkat/l a TG 1,9 mmo/l. Výrazně poklesla i hodnota celkového cholesterolu na 9,8 mmol/l a GMT na 5,37 μkat/l, téměř normě se blížila hodnota ALT 1,11 ukat/l. Po výrazném poklesu hemoglobinu (89,4 g/l) při akutní hemolytické anémii došlo k pozvolnému zvýšení těchto hodnot (106 g/l) v průběhu 2. a 3. týdne terapie bez nutnosti podání krevní transfuze. Vývoj laboratorních hodnot v časovém horizontu od přijetí po dobu 3 týdnů (chol, TG, bili, kojugovaného bili, AST, ALT, GMT, ALP, a Hb) je dokumentován v grafech 1 až 4.
DISKUZE
Náhlá příhoda břišní s paralytickým ileózním stavem může být první příčinou vyšetření nemocných se Zieveho syndromem, její vznik lze vysvětlit poruchou vnitřního prostředí, která po substituční terapii spontánně odezní. Bolest břicha může vést až k provedení diagnostické laparotomie. Diagnostiku Zieveho syndromu pak podpoří žloutenka, hemolytická anémie, hyperbilirubinémie, jaterní dysfunkce a anamnéza alkoholického excesu (pokud ji pacient přiznává)(1,2). V bioptickém nálezu je pak charakteristická velkokapénková steatóza či steatohepatitida často bez přechodu do cirhózy(4).
Diagnostika Zieveho syndromu u nemocných s jaterní cirhózou po alkoholickém exscesu, provázená hypercholesterolémií a hemolytickou anémií, probíhající často pod obrazem cholestatické alkoholické hepatitidy, může podporovat alkoholický původ jaterního postižení (i v případě, že pacient pravidelný příjem alkoholu popírá). Po abstinenci pacientů je rovněž charakteristická poměrně rychlá úprava laboratorních parametrů i klinického stavu(8-11).
Mechanizmus hemolýzy není přesně znám. Zieve předpokládal, že abnormální cirkulace lipidů zvyšuje nestabilitu membrány červených krvinek, a tím je predisponuje k hemolýze. Tato teorie však nebyla potvrzena(1). Do roku 2003 bylo popsáno přibližně 200 případů hemolytické anémie ve spojení se Zieveho syndromem(11).
Nejnápadnějším a většinou prvním laboratorním příznakem tohoto syndromu je mléčně zkalené sérum. Jeho příčinou je hyperlipidémie. Stupeň mléčně zkaleného séra je závislý na přísunu alkoholu a po jeho vysazení se i sérum postupně vyjasňuje(9). Pokud nemocný nedodržuje abstinenci, může dojít k znovuobjevení jak subjektivních, tak objektivních známek onemocnění(11).
ZÁVĚR
Zieveho syndrom je charakterizován žloutenkou, hemolytickou anemií, hyperlipidémií a jaterní dysfunkcí spojenou s abúzem alkoholu. U pacientů může probíhat i pod obrazem náhlé příhody břišní se subileózním až ileózním stavem jako v našem případě. Konzervativní terapie spočívající v dietním omezení s dostatečným přísunem vitaminů a stopových prvků vede k postupné úpravě subjektivního stavu i laboratorních hodnot.
 LITERATURA
LITERATURA
- 1. Zieve L. Jaudince, hyperlipidaemia and haemolytic anaemia: a heretofore unrecognised syndrome associated with alcoholic fatty liver and cirrhosis. Ann Intern Med 1954; 48: 471-496.
- 2. Ehrmann J. Komplikace jaterní cirhózy. In Ehrmann J, jr., Schneiderka P, Ehrmann J. Alkohol a játra, 1. vyd. Praha: Grada Publishing 2006; 88-110.
- 3. Martin JC, Ross A, Watson D, O'Sullivan MM. A case of Zieves syndrom presenting with myalgia: not to be confused with polymyalgia rheumatica. British Journal of rheumatology 1995; 35: 495-496.
- 4. Goebel KM. Red cell metabolism in transient haemolytic anaemia associated with Zieves syndrome. European Journal of Clinical Investigation, 1975, 5, 83-91.
- 5. Heermans EH. Booze and blood. The effects of acute and chronic alcohol abuse on the hematopoietic system. Clin Lab Sci 1998; 11: 229-233.
- 6. Fernandez Perez FJ, Pallares Manrique H, Cabello Ramirez M, et al. Zieve's syndrome. A case report. Revista Espanola de Enfermedades Digestivas 1996; 88: 226-229.
- 7. Esrailian E, Saab S. Hematopoietic abnormalities and hemostasis. In: Boyer TD, Wright TL, Manns MR Zakim and Boyer's hepatology A textbook of liver disease Saunders - Elsevier 2006; 489-499.
- 8. Ehrmann J. Souhrn - základní kritéria diagnostiky alkoholického postižení jater. In Ehrmann J, jr., Schneiderka P, Ehrmann J. Alkohol a játra. Praha: Grada Publishing 2006; 137-141.
- 9. Vavroš B, Dostalík Z. Zieveho syndrom. Vztah ke klinicko-patologickým formám alkoholových onemocnění jater u čtyř vlastních pozorování. Vnitř Lék 1973; 19: 1117-1129.
- 10. Dvořák V, Oškera J. Zieveho syndrom. Česk Gast-roenterol Výž 1970; 24: 368-372.
- 11. Puccini J, Haldar S, Jefferson B. Case from the Osier Medical Service at Johns Hopkins University. Am J Med 2003; 11: 729-731.
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené