Závažné krvácanie ako komplikácia endoskopickej choledocho-duodenálnej drenáže prostredníctvom lumen apozičného stentu (Hot-Axios) v riešení distálnej stenózy ductus choledochus pri adenokarcinóme hlavy pankreasu
Roman Belica1, Denisa Kudlová1, Andrej Klepanec2, Matúš Hoferica2, Ján Haršány2, Ján Rajec1, Martin Habiňák1, Rastislav Husťak1,3, Jan Martínek1,3
+ Pracoviště
Souhrn
Úvod:
Endoskopická transpapilárna drenáž je obvyklou metódou riešenia malígnej biliárnej obštrukcie. Alternatívou transpapilárneho prístupu je endosonograficky navigovaná biliárna drenáž pomocou lumen apozičného stentu, ktorú možno využiť nielen pri zlyhaní ERCP.
Kazuistika:
Opisujeme našu skúsenosť s endosonograficky navigovanou choledocho-duodenálnou drenážou pomocou lumen apozičného stentu, ktorá bola komplikovaná oneskorenou hemobíliou. Perzistujúce a závažné krvácanie bolo úspešne vyriešené endovaskulárnou embolizáciou pomocou špirál.
Záver:
Endosonograficky navigované drenáže pomocou lumen apozičného stentu môžu byť, napriek všetkým svojim výhodám, sprevádzané závažnými komplikáciami vrátane významného krvácania, preto je vhodná dostupnosť pracoviska intervenčnej rádiológie.
Klíčová slova
endosonografia, endoskopická retrográdna cholangiopankreatikografia, pankreas, cholestáza, obštrukčný ikterus, adenokarcinóm
Digestívna endoskopia: kazuistika
Úvod
Nebolestivý obštrukčný ikterus je častou komplikáciou u pacientov s malígnymi nádormi v oblasti hlavy pankreasu, často sa jedná o prvý príznak ochorenia. V prípade tejto diagnózy je zásadným krokom posúdenie resekability nálezu, k čomu prispieva hlavne multidetektorová počítačová tomografia (CT) a v druhom kroku je obvykle doplňovaná endosonografia (EUS). V závislosti od výsledkov stagingu sa potom odvíja i riešenie obštrukčného ikteru. V prípade operabilného nálezu je primárnou terapeutickou voľbou resekčný výkon, pričom predoperačná biliárna drenáž nie je (pri absencii cholangitídy) nevyhnutná, jej zavedenie je totiž spojené s vyšším rizikom pooperačných komplikácií. V prípade inak symptomatického ikteru (cholangitída, pruritus) a nemožnosti skorej operácie (v priebehu dní), je väčšinou indikované ERCP vyšetrenie so zavedením duodeno-biliárnej transpapilárnej drenáže. Ak ide o inoperabilný nález, drenáž je nevyhnutná nielen pred začatím eventuálnej paliatívnej či inej onkologickej terapie, ale je indikovaná aj ako paliatívna liečba ikteru [1]. V prípade neúspechu ERCP (stenóza duodena, neúspešná kanylácia žlčových ciest, nemožnosť prieniku zavádzača cez stenózu) bola väčšinou indikovaná transhepatálna drenáž (PTD).
V posledných rokoch sa do praxe zaviedli tzv. lumen apozičné metalické stenty (LAMS), umožňujúce elegantnú EUS navigovanú drenáž pankreatických tekutinových kolekcií, i žlčových vývodov či gastroenteroanastomóz [2–4]. Vďaka tomu je pri zlyhaní ERCP možné vykonať EUS navigovanú bilio-duodenálnu drenáž, ktorej výhodou oproti PTD nie je len absencia perkutánneho prístupu. Počas EUS je možné v jednej dobe posúdiť detailné lokoregionálne zmeny, pokiaľ je nádor zjavne pokročilý (napr. invázia veľkých artérií), možno súčasne vykonať ako histologickú diagnostiku (FNAB), tak aj EUS navigovanú drenáž, a pacient je tak ušetrený od ďalšieho invazívneho endoskopického zákroku [5].
Medzi ojedinelú, ale život-ohrozujúcu komplikáciu EUS navigovanej drenáže, patrí krvácanie. Formou kazuistiky prezentujeme klinický prípad úspešného zvládnutia závažného krvácania po EUS navigovanej biliárnej drenáži.
Popis prípadu
Pacientka (71 rokov) bola odoslaná s nebolestivým obštrukčným ikterom (bilirubín: 76,3 μmol/l, GMT 29,6 μkat/l, ALP 5,1 μkat/l) v dôsledku tumoru hlavy pankreasu na gastroenterologické pracovisko Kliniky vnútorného lekárstva FN Trnava v období pandémie covid-19 k ďalšiemu stagingu a zváženiu terapie. Podľa údajov v osobnej anamnéze bola pacientka po hysterektómii a adnexektómii pre včasný karcinóm krčka maternice (1997), po adenokarcinóme pľúc riešeným resekciou ľavého laloka pľúc (2019) a st. p. bazocelulárnom karcinóme viečka.
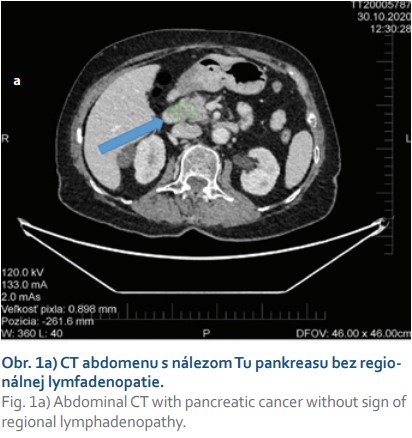
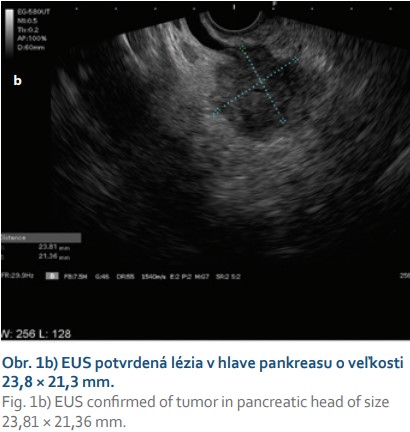
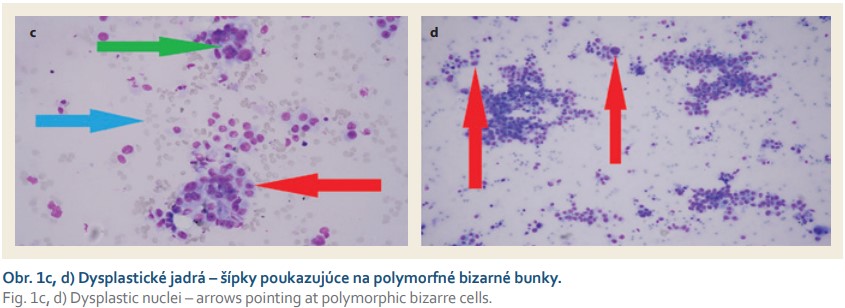
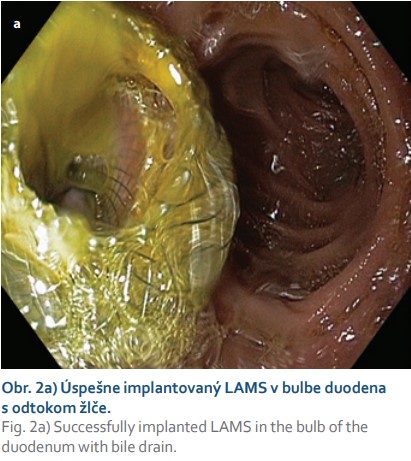
Na vstupnom CT abdomenu (obr. 1a) a následnom multiodborovom seminári bol tumor zhodnotený ako operabilný, no pacientka s operačným postupom jednoznačne nesúhlasila. Následne pri EUS bola nájdená hypoechogénna neostro ohraničená lézia (obr. 1b) v oblasti hlavy pankreasu bez invázie do lokálnych cievnych štruktúr, bez lymfangioinvázie. Doplnená bola FNB (Acquire 22G, Boston Scientific), on-site patológ potvrdil prítomnosť adenokarcinómu v cytologickom a neskôr aj histologickom rozbore (obr. 1c, d). Po odbere tkanivovej vzorky sme sa rozhodli realizovať biliárnu drenáž a ako najvhodnejšia bola zvolená duodenálna pozícia v apexe bulbu (obr. 2a). Po vylúčení interpozície veľkých ciev a pri dobrom diametri choledochu pri EUS kontrole bol transduodenálne zavedený LAMS (10 × 10 mm HOT-AXIOSTM) do distálneho choledochu pod odstup pahýľu cystiku. Po rozvinutí distálneho a proximálneho krídla stentu bol pozorovaný odtok stagnačnej žlče. Výkon bol realizovaný na endoskopickom pracovisku bez simultánnej potreby RTG kontroly, v monitorovanej celkovej anestézii, v trvaní asi 15 minút. Periprocedurálne boli profylakticky podané antibiotiká v jednorazovej dávke (penicilín) a pacientka bola uložená na lôžko k odsledovaniu.
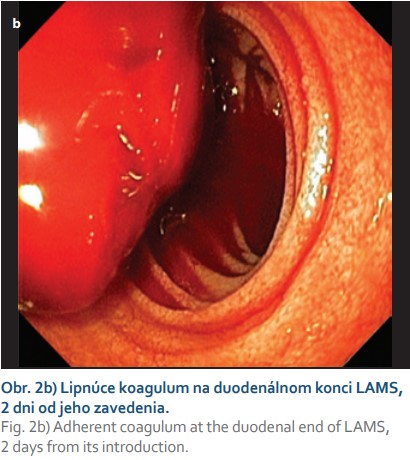
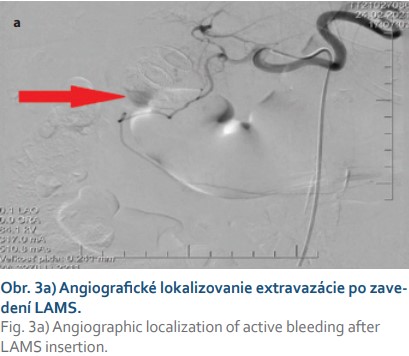
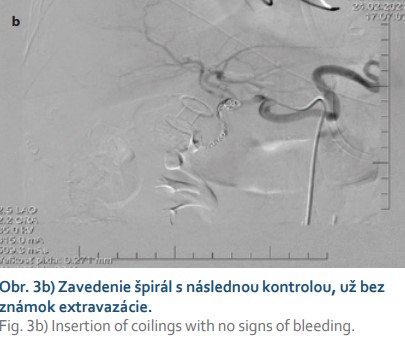
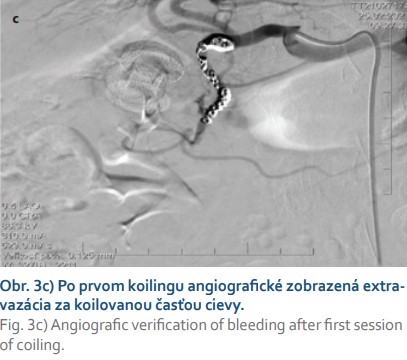
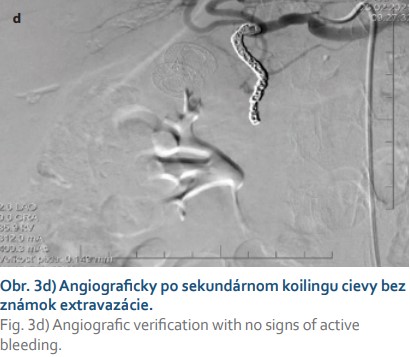
U pacientky sa po 6 hodinách od výkonu objavili bolesti na hrudníku s pozitívnou kardiošpecifickou humorálnou odpoveďou (TNI 80,1; o 3 hodiny 582,4) a de novo záchytom fibrilácie predsiení (FA). Pre akútny koronárny syndróm bola preložená na Národný ústav srdcových a cievnych chorôb, kde na echokardiografii neboli pozorované regionálne známky poruchy kinetiky. Pre riziko tyreotoxicity u pacientky so známou subklinickou hypertyreózou nebola koronarografia indikovaná. Pre FA bola pacientka nastavená na antikoagulačnú liečbu (nízkomolekulový heparín) s duálnou protidoštičkovou liečbou (DAPT, aspirín + klopidogrel). Následne po 2 dňoch bola preložená z Národného ústavu srdcových a cievnych chorôb späť na naše pracovisko k doriešeniu stavu. Pacientka bola pri prijatí anikterická, so signifikantným poklesom cholestázy (bilirubín: 15,1 μmol/l; GMT: 9,6 μkat/l; ALP: 7,1 μkat/l). V ďalšom veľmi krátkom priebehu sme zaznamenali klinicky významné krvácanie vo forme melény. Endoskopicky sa verifikovalo krvácanie z oblasti duodenálneho konca LAMS (obr. 2b), ktoré endoskopista riešil opichom 1% adrenalínu, pauzovala sa DAPT a pokračovalo sa parenterálnym podávaním inhibítorov protónovej pumpy spolu s profylaktickou dávkou nízkomolekulového heparínu. Po 12 hodinách od ošetrenia a pri prejavoch pokračujúceho krvácania bolo realizované CT angiografické vyšetrenie, kde bol vizualizovaný leak kontrastnej látky z vetvy a. gastroduodenalis pri choledochálnom konci LAMS (obr. 3a). Konzultovaný intervenčný rádiológ realizoval embolizáciu a. gastroduodenalis implantáciou 9 špirál (obr. 3b). Po 24 hodinách bolo pozorované opätovné krvácanie (obr. 3c), kedy bola znovu vykonaná digitálna subtrakčná angiografia (DSA) a ďalšia embolizácia a. gastroduodenalis implantáciou piatich špirál s následným uzáverom a. gastroduodenalis a dobrým klinickým efektom bez ďalšieho poklesu na hemograme (obr. 3d).
Celkovo bolo pacientke podaných sedem transfúzií. Po prolongovanej hospitalizácii (12 dní) bola pacientka prepustená do domácej starostlivosti. Vzhľadom na onkologický nález podstupuje systémovú onkologickú liečbu a s chirurgickým riešením nesúhlasí. V závere ako príčinu krvácania možno predpokladať najskôr dekubit v stene duodenocholedochálnej fistuly po zavedení LAMS v kombinácii s nastavením na duálnu antitrombotickú liečbu.
Diskusia
Prvou metódou voľby riešenia distálnej obštrukcie žlčových ciest pri tumore pankreasu neindikovanom k resekcii je považovaná ERCP so zavedením plastového alebo kovového stentu [1]. V prípade nedostupnosti papily z dôvodu napr. stenózy duodena alebo neúspešnej kanylácie papily, bola a stále aj je ako „zlatá metóda“ na mnohých pracoviskách preferovaná perkutánna transhepatálna drenáž (PTD) [4]. Efektivita ERCP drenáže je vysoká v terciárnych centrách (86–95 %) [1]. Na druhej strane je PTD spojené s rizikom komplikácií (23 %), najčastejšie dysfunkcia drenáže (dislokácia/obturácia), infekčné či krvácavé komplikácie [6].
Rozvojom endosonografie a možnosti zavedenia LAMS do praxe sa výrazne zvýšila efektívnosť luminálnej biliodigestívnej drenáže v jednokrokovom postupe. EUS navigované biliogastrické (BG) alebo bilioduodenálne (BD) drenáže sa v dnešnej dobe stali súčasťou algoritmu riešenia komplexných biliárnych stenóz [5]. Prvé EUS-BD drenáže boli realizované plastovými stentami, ale vysoká miera biliárnych leakov a peritonitíd bránili ich širšiemu využitiu [7]. Na druhej strane, incidencia komplikácií pri EUS-biliodigestívnych drenážach s LAMS nie je nulová (17 %) a najčastejšie sa vyskytujú krvácavé komplikácie, resp. technické problémy s uvoľňovaním stentu, alebo jeho priechodnosťou [8]. Novou myšlienkou biliárnych drenáží je EU-RCP (kombinácia EUS a ERCP v jednej procedúre), ktoré napr. z dôvodu možných technických komplikácií s rozvíjaním LAMS, je vhodné, aby sa realizovalo s dostupnosťou röntgenovej kontroly. Novým míľnikom (krátkej) budúcnosti je využívanie LAMS pri EUS BD ako primárnej drenážnej metódy pri distálnej biliárnej stenóze. Dokonca i v randomizovanej štúdii mala EUS-DB vs. ERCP porovnateľnú efektivitu (97,0 vs. 91,2 %; p = 0,61), s podobnou mierou komplikácií (21,2 vs. 14,7 %; p = 0,49), [9].
V našom prípade sa jednalo o malígnu biliárnu stenózu pri adenokarcinóme hlavy pankreasu, ktorá mala vhodné podmienky k EUS drenáži (choledochus šírky 16 mm) bezprostredne po FNB daného ložiska. V danej situácii bolo (s akceptáciou rizík a benefitov pre pacientku) preferované zavedenie LAMS a od „klasickej“ ERCP bolo upustené. Periprocedurálne po aplikácii LAMS neboli dokumentované žiadne komplikácie. Bezprostredne po začatí kombinovanej antitrombotickej liečby pre akútny koronárny syndróm, bol stav komplikovaný melénou s objektivizáciou lipnúceho koagula s presakovaním krvi na duodenálnom konci LAMS. V diferenciálnej diagnostike bolo nutné vylúčiť prítomnosť portobiliárnej fistuly CT angiografiou a následne endoskopicky neošetriteľné pokračujúce krvácanie riešiť transarteriálnou embolizáciou, ktorá je zároveň prvou metódou voľby v liečbe hemobílie. Jej efektivita je vysoká a dosahuje 80–100 %. Ideálnym spôsobom uzáveru leaku z poškodenej cievy je koiling, alternatívou môže byť i použitie lepidla [10].
Krvácavé komplikácie boli dokumentované vo viacerých štúdiách s LAMS, hlavne pri drenáži pankreatických kolekcií. V súčasnosti sa EUS-BD javí ako vhodná alternatíva prvej voľby u pacientov s pozmenenou luminálnou anatómiou a ťažko dostupnou papilou [11]. V blízkej budúcnosti budú potrebné cost-benefit analýzy takýchto postupov. Výhodami EUS-BD je lepšia tolerancia výkonov pacientmi pre absenciu externého vývodu (sú ale možné PTD s inzerovaním metalického biliárneho stentu ako paliatívneho riešenia), jedno-krokovosť výkonu zavedenia LAMS, pri technicky správnej realizácii je nízke riziko post-procedurálnej pankreatitídy a iné [12]. Dôsledné zhodnotenie rizík krvácania, prípadne úprava antitrombotickej a antikoagulačnej liečby môže znížiť riziko krvácavých komplikácií. V našom prípade mala pacientka zavedenú tripletnú terapiu. Nevyzretá choledochoduodeálna fistula po LAMS v kombinácii s antitrombotickou liečbou a možným dekubitom v stene duodenocholedochálnej fistuly participovali na závažnom krvácaní.
Záver
Kazuistikou chceme upozorniť v prvom rade na nový postup v riešení malígnej distálnej obštrukcie pomocou EUS navigovanej LAMS drenáže. Dôležitým druhým aspektom je realizácia výkonu skúseným/trénovaným endoskopistom pre technicky náročný výkon a obzvlášť na pracovisku s okamžitou možnosťou rádiologickej či chirurgickej intervencie pri prípadných komplikáciách.
Doručené/Submitted: 19. 5. 2021
Prijaté/Accepted: 6. 6. 2021
MUDr. Roman Belica
Klinika vnútorného lekárstva FN Trnava
A. Žarnova 11
917 02 Trnava
belica.roman@gmail.com
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Dumonceau JM, Tringali A, Papanikolaou IS et al. Endoscopic biliary stenting: indications, choice of stents, and results: European Society of Gastrointestinal Endoscopy (ESGE) Clinical Guideline – Updated October 2017. Endoscopy 2018; 50(9): 910–930. doi: 10.1055/a-0659-9864.
2. Mussetto A, Fugazza A, Fuccio L et al. Current uses and outcomes of lumen-apposing metal stents. Ann Gastroenterol 2018; 31(5): 535–540. doi: 10.20524/aog.2018.0287.
3. Bang JY, Navaneethan U, Hasan M et al. Stent placement by EUS or ERCP for primary biliary decompression in pancreatic cancer: a randomized trial (with videos). Gastrointest Endosc 2018; 88(1): 9–17. doi: 10.1016/j.gie.2018.03.012.
4. Brountzos EN, Ptochis N, Panagiotou I et al. A survival analysis of patients with malignant biliary strictures treated by percutaneous metallic stenting. Cardiovasc Intervent Radiol 2007; 30(1): 66–73. doi: 10.1007/s00270-005-0379-3.
5. Pedersoli F, Schröder A, Zimmermann M et al. Percutaneous transhepatic biliary drainage (PTBD) in patients with dilated vs. nondilated bile ducts: technical considerations and complications. Eur Radiol 2021; 31(5): 3035–3041. doi: 10.1007/s00330-020-07368-6.
6. Tsuchiya T, Teoh AYB, Itoi T et al. Long-term outcomes of EUS-guided choledochoduodenostomy using a lumen-apposing metal stent for malignant distal biliary obstruction: a prospective multicenter study. Gastrointest Endosc 2018; 87(4): 1138–1146. doi: 10.1016/j.gie.2017.08.017.
7. Leung Ki EL, Napoleon B. Endoscopic ultrasound-guided biliary drainage: A change in paradigm? World J Gastrointest Endosc 2019; 11(5): 345–353. doi: 10.4253/wjge.v11.i5.345.
8. Papadopoulos P, Bize P, Guiu B et al. Percutaneous transhepatic stent graft placement for treatment of hepatic artery injury after a Whipple procedure. J Vasc Interv Radiol 2014; 25(6): 977–978. doi: 10.1016/j.jvir.2014.03.020.
9. Hathorn KE, Bazarbashi AN, Sack JS et al. EUS-guided biliary drainage is equivalent to ERCP for primary treatment of malignant distal biliary obstruction: a systematic review and meta-analysis. Endosc Int Open 2019; 7(11): E1432–E1441. doi: 10.1055/a-0990-9488.
10. Leung Ki EL, Napoleon B. Endoscopic ultrasound-guided biliary drainage: A change in paradigm? World J Gastrointest Endosc 2019; 11(5): 345–353. doi: 10.4253/wjge.v11.i5.345.
11. Papadopoulos P, Bize P, Guiu B et al. Percutaneous transhepatic stent graft placement for treatment of hepatic artery injury after a Whipple procedure. J Vasc Interv Radiol 2014; 25(6): 977–978. doi: 10.1016/j.jvir.2014.03.020.
12. Hathorn KE, Bazarbashi AN, Sack JS et al. EUS-guided biliary drainage is equivalent to ERCP for primary treatment of malignant distal biliary obstruction: a systematic review and meta-analysis. Endosc Int Open 2019; 7(11): E1432–E1441. doi: 10.1055/a-0990-9488.