Význam domácej parenterálnej výživy v klinickej praxi – vlastné skúsenosti z nášho centra
Andrea Fojtová1, Barbora Norek1, Katarína Gazdíková2
+ Pracoviště
Souhrn
Domáca parenterálna výživa je náhradnou cestou a formou výživy u pacientov s ireverzibilným zlyhaním intestinálnych funkcií, u ktorých enterálna výživa nie je možná, resp. dlhodobo nedostačujúca s prehlbujúcim sa energetickým deficitom. Zahájením parenterálnej výživy v domácom prostredí sa zlepšuje kvalita života pacientov, a tým aj priebeh základného ochorenia s optimalizáciou klinických prejavov malnutrície. K najčastejším indikáciám domácej parenterálnej výživy patria rozsiahle redukcie absorbčnej plochy pri intestinálnych resekciách (pri chirurgických komplikáciách morbus Crohn, pri ischemickej nekróze tenkého čreva v dôsledku trombózy vo vena mesenterica superior, resp. embólii alebo aterosklerotickom uzávere arteria mesenterica superior, ale tiež funkčné zlyhanie čreva rôznej etiológie a nádorové ochorenia s dostatočnou utilizáciou základných živín).
Klíčová slova
domáca parenterálna výživa, syndróm krátkeho čreva, komplikácie
Úvod
Zahájenie klinickej výživy (parenterálnej aj enterálnej) by malo byť súčasťou komplexnej liečby pacientov so zistenou malnutríciou pri črevnom zlyhaní rôznej etiológie. Domáca parenterálna výživa (DPV) a hydratácia sa najčastejšie nasadzujú u pacientov s ireverzibilným zlyhaním čreva, s trvalou potrebou parenterálnej substitúcie základných živín, elektrolytov, vitamínov a stopových prvkov.
Domáca parenterálna výživa
DPV je súbor medicínskych úkonov realizovaných edukovaným pacientom, príbuzným alebo agentúrou domácej ošetrovateľskej starostlivosti (ADOS) v domácom prostredí, u ktorého nie je možné zabezpečiť adekvátnu nutričnú potrebu per vias naturales ani s pridaním medicínsky definovanej stravy – enterálnej výživy. Je realizovaná podávaním vakov „all in one“ s definovaným množstvom tukov, cukrov, bielkovín a aditív – elektrolytov, stopových prvkov a vitamínov. Aplikuje sa pacientom, u ktorých nie je možné naplniť nutričné požiadavky orálnou alebo enterálnou cestou a nie je iný dôvod pokračovať v hospitalizácii. Ďalšími podmienkami je schválenie zdravotnou poisťovňou na uhrádzanie z verejného zdravotného poistenia a absolvovanie tréningu v DPV a overenie spôsobilosti pacienta a jeho príbuzného/príbuzných v aplikácii výživových roztokov [1].
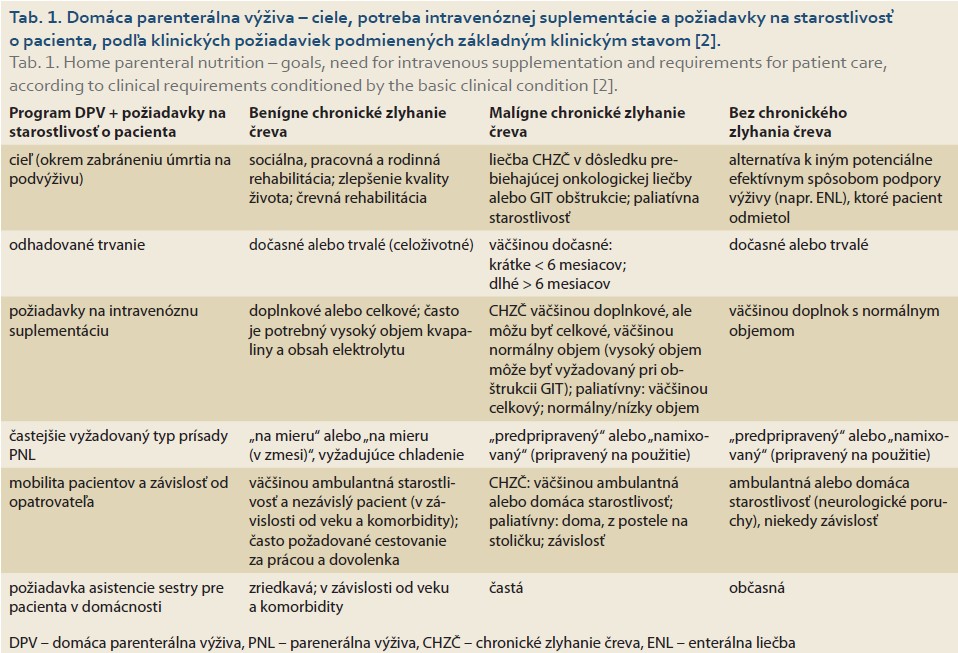
DPV umožňuje celému spektru pacientov zlepšiť nielen kvalitu, ale aj dĺžku života, na druhej strane okrem priaznivého účinku na zdravotný stav pacienta so zlyhaním tráviaceho traktu, žiaľ existuje viacero komplikácií, asociovaných s jej aplikáciou. Ciele a požiadavky na DPV aktualizované podľa guidelines pre DPV a podmienky na realizáciu DPV sú uvedené v tab. 1 [2].
Medzi indikácie DPV patria pacienti odkázaní na dlhodobý príjem živín parenterálnou cestou a základné ochorenie si nevyžaduje hospitalizáciu, choroby gastrointestinálneho traktu (GIT, malabsorpcia – syndróm krátkeho čreva [SBS], chronické intestinálne pseudoobštrukcie, cystická fibróza s ťažkou malnutríciou, závažné postihnutie čreva pri morbus Crohn), onkologické ochorenia s rozvojom malnutrície.
Pacienti sú zaradení do programu DPV na základe splnenia kritérií stanovených v Odbornom usmernení organizácie klinickej výživy č. 13163/2006 v znení Odborného usmernenia č. 06242/2008-OZS, vydanom vo Vestníku MZ, čiastka 1–3/2009 [3].
Kritériá zaradenia do DPV rozdeľujeme na medicínske, nutričné, biosomatické a psychosociálne.
a) Medicínske kritériá – zlyhanie resorpčných funkcií tenkého čreva (tab. 2). Patria sem:
1. rozsiahla redukcia absorpčnej plochy – SBS po rozsiahlych intestinálnych resekciách, pri chirurgických komplikáciách, Crohnovej chorobe, pri ischemickej nekróze tenkého čreva v dôsledku trombózy vena mesenterica superior, pri embólii alebo aterosklerotickom uzávere arteria mesenterica superior a po resekciách z iných príčin;
2. malabsorpcia pri ireverzibilnom poškodení intestinálnej mukózy – pri pokročilej sklerodermii, pri kongenitálnych defektoch a pri postradiačnej enteropatii;
3. závažné poruchy pasáže GIT (posudzuje sa pokročilosť a závažnosť klinického stavu, sprevádzajúce choroby, fyzická kondícia a mentálny stav pacienta, schopnosť spolupracovať) – pri karcinomatóze peritonea, pri inoperabilných malígnych chorobách GIT a pri pseudoobštrukcii.

b) Nutričné kritériá – hodnotí sa závažnosť malnutrície, prítomnosť deficitných syndrómov, reverzibilita metabolických porúch, individuálne nutričné požiadavky a overuje sa možnosť kombinovanej enterálnej a parenterálnej výživy.
c) Biosomatické kritériá – stav koagulácie, údaje o trombotických príhodách, morfologický stav centrálneho cievneho systému, údaje o minulých kanyláciách, epidemiologické údaje o prekonanej sepse a bakteriálnej endokarditíde a priechodnosť centrálnych žíl.
d) Psychosociálne kritériá – liečba je časovo náročná a predstavuje záťaž pre celú rodinu. Pacient i rodina vyjadria písomný súhlas s DPV, sú poučení o obsluhe a rizikách, ovládajú samostatné riešenie vzniknutých problémov. Preverujú sa hygienické návyky a hygienické vlastnosti domáceho prostredia [1].
Zahájením DPV pri benígnych ochoreniach je možné dosiahnuť reverzibilitu črevného zlyhania v 20–50 % v priebehu 1–2 rokov [4]. Pri pokročilých nádorových ochoreniach je zahájenie DPV kontroverzné [5]. Pracovná skupina ESPEN neodporúča zahájenie DPV u pacientov s predpokladanou dĺžkou života menej ako 3 mesiace [6]. Ďalšie rozhodovanie o nasadení DPV u onkologických pacientov je na základe zhodnotenia stupňa utilizácie základných živín a miery sebestačnosti pacienta (Karnofského skóre viac ako 50 bodov). Patofyziologická klasifikácia črevného zlyhania definuje širokú škálu najčastejších príčin indikácie DPV (tab. 3) a napomáha medziodborovej komunikácii a schvaľovaniu žiadostí zdravotnou poisťovňou.

Komplikácie DPV
Komplikácie vzniknuté v súvislosti s DPV sa riešia v centre DPV a sú uvedené v tab. 4 [1].

Najčastejšou príčinou hospitalizácie pacientov na DPV patrí katétrová sepsa [7]. Zdrojom infekcie sú najčastejšie baktérie z kože v okolí katétra a baktérie, ktoré sa dostanú do katétra pri nesprávnej manipulácii z rúk, nosa a úst. Menej často sa jedná o endogénne infekcie a zriedkavo o aplikáciu kontaminovaného roztoku. Z etiologických agensov sú to majoritne Staphylococcus epidermidis a koaguláza negatívne stafylokoky, ktoré zodpovedajú za približne 37 % katétrových infekcií a často preukazujú značnú rezistenciu na antistafylokokové antibiotiká. Enterokoky postihujú pacientov so zníženou imunitou a tvoria asi 16 %, pričom zvyčajne pochádzajú z endogénnej flóry alebo nemocničného prostredia. Kvasinkové infekcie sú zodpovedné za 8 % infekčných katétrových komplikácií. Enterobacter, Escherichia coli, Klebsiella pneumoniae a Pseudomonas aeruginosa sú zriedkavejší pôvodcovia, avšak ich zvýšený záchyt bol zistený u pacientov so syndrómom krátkeho čreva, kde sa predpokladá porušenie črevnej bariéry. Spoločnou vlastnosťou mikroorganizmov zodpovedných za katétrové infekcie je schopnosť tvoriť biofilm [8,9]. Antibiotická liečba má byť včasná a cielená, v dostatočnej dávke, podávaná minimálne 10 až 14 dní. Jej úspešnosť závisí od druhu patogénu, jeho virulencie a od adekvátnej liečby. Cieľom liečby je eradikovať infekciu, udržať funkčný katéter a zabrániť recidívam infekcie. Nezvládnutie katétrovej sepsy je indikáciou na extrakciu katétra. Treba si uvedomiť, že časté výmeny katétra devastujú centrálny žilový systém [10].
Katétrovej sepse je možné predchádzať už pri implantácii cievneho prístupu. Dlhodobý centrálny žilový katéter alebo port má zavádzať erudovaný lekár pod ultrasonografickou kontrolou, aby sa zamedzilo opakovanej punkcii a nadmernému tkanivovému poškodeniu [10]. Najdôležitejšou zložkou prevencie infekčných komplikácií je tréning pacienta v programe DPV, prípadne jeho príbuzného. Edukáciu vykonáva katétrová sestra. Ako pomôcka na výučbu slúži v centrách pre DPV na Slovensku Manuál pre pacienta na DPV, rôzne modelové pomôcky a tréningové video s kompletnou inštruktážou [11].
Ochranná katétrová zátka sa používa na bezpečné preplachovanie a uzatváranie dlhodobých cievnych vstupov. Má redukovať možnosť vzniku biofilmu a kolonizácie katétra, a tým znížiť incidenciu katétrovej sepsy. Okrem toho má ochrániť katéter pred intraluminálnou obštrukciou. V rutinnej starostlivosti o dlhodobý CVK je po dotečení terapie postačujúce prepláchnutie a uzamknutie katétra fyziologickým roztokom na obdobie katétrového pokoja [10]. V minulosti používaná heparínová zátka nemá podľa metaanalýz v prevencii katétrovej sepsy väčší efekt ako fyziologický roztok. Od jej aplikácie sa upustilo najmä po potvrdení podpory rastu biofilmu pri katétrovej infekcii spôsobenej Staphylococcus aureus. Stále sa používa pri starostlivosti o žilové katétre [10,12]. Na prevenciu infekčných komplikácií a obštrukcie, do dlhodobých cievnych vstupov pre DPV u pacientov s vysokým rizikom vzniku infekčných komplikácií, sa ako zátka používa roztok taurolidínu so širokými antimikrobiálnymi a antimykotickými vlastnosťami, s účinnosťou aj na meticilín a vankomycín rezistentné kmene, ktorý zabraňuje aj tvorbe biofilmu a kolonizácii katétra [1,13]. V prevencii katétrovej sepsy nie sú účinné neindikované výmeny katétrov, profylaktické podávanie antibiotika pred alebo počas používania katétra, antibiotické zátky ako profylaxia [14].
Z metabolických komplikácií okrem oxalátovej nefropatie pri SBS je častý výskyt steatózy pečene, ktorá sa vyskytuje pri vysokom prívode glukózy, nedostatku esenciálnych mastných kyselín a pri nadmernom prívode triacylglycerolov a nedostatku karnitínu. K ďalším príčinám vzniku steatózy patria aj aplikácia hepatotoxických liekov, sepsa, biliárna obštrukcia a bakteriálna translokácia [15]. Preto je potrebný konštantný prívod energie (25–35 kcal/kg telesnej hmotnosti [TH]/deň), proteínov (0,8–1,5 g/kg TH/deň), sacharidov (3–6 g/kg TH/deň), tukov (max. 1 g/kg/deň). U pacientov, ktorým je podávaných parenterálnou výživou viac ako 35 kcal/kg TH, hrozí riziko vzniku overfeeding syndrómu, ktorého dôsledkom je hyperkapnia, zvýšená pečeňová lipogenéza, hyperglykémia, abnormality metabolizmu elektrolytov, porušená fagocytóza a zvýšená energetická spotreba [1]. Dôležitosť podávania vitamínov, stopových prvkov, resp. substitúcia iónov spočíva v prevencii vzniku deficitných syndrómov (napr. Wernickeho encefalopatia pri deficite thiamínu). Osteopénia pri dlhodobom podávaní parenterálnej výživy sa vyskytuje cca u 41–46 % pacientov, preto je potrebná substitúcia vitamínu D, vápnika a fosfátov v roztokoch [1].
Alternatívne riešenia pri dlhodobej DPV
Z ďalších liečebných možností pri črevnom zlyhaní, za dodržania indikácií, je aj použitie analógu glukagón-like peptidu, ktorý zvyšuje prietok krvi črevami a portálny prietok krvi, inhibuje sekréciu žalúdočnej kyseliny a znižuje motilitu čreva. K ďalšiemu alternatívnemu riešeniu radíme transplantáciu tenkého čreva, ktorá sa dnes považuje za jediné dlhodobé riešenie pre pacientov so zlyhaním čreva, u ktorých došlo k závažným komplikáciám pri dlhodobej parenterálnej výžive (tab. 4). Prvú transplantáciu tenkého čreva vykonal v roku 1967 prof. Liliheim so spolupracovníkmi. Vďaka pokroku v imunosupresívnej liečbe, v operačnej technike a pooperačnej starostlivosti počet úspešných transplantácií tenkého čreva stúpa. Počet kandidátov na transplantáciu tenkého čreva sa neustále zvyšuje a väčšinou sa jedná o mladších pacientov. Najčastejšou indikačnou príčinou na transplantáciu tenkého čreva je SBS.
Činnosť nášho strediska DPV
Na Slovensku funguje 10 centier DPV, ktoré v roku 2019 evidovali celkovo 127 pacientov (dospelých aj detských) [16].
Naše centrum DPV bolo zriadené v novembri 2012 ako súčasť Gastroenterologickej (GAE) kliniky Univerzitnej nemocnice v Bratislave (Petržalka), so súhlasom MZ SR, s podmienkou zabezpečenia posteľovej bázy v rámci GAE kliniky pri zahájení DPV, edukácii pacienta a jeho rodinných príslušníkov ako aj pre prípad komplikácií súvisiacich s DPV.
Stredisko DPV zabezpečuje:
a) ordináciu potrebných nutričných prípravkov a pomôcok,
b) pravidelné kontroly nutričného i celkového klinického stavu pacientov,
c) riešenie komplikácií.
Pri zaraďovaní pacientov do programu DPV sa posudzuje ich celkový klinický stav, rozsah malfunkcie GIT-u a nutričné potreby organizmu. Pred zaradením je pacient podrobne informovaný o charaktere liečby, možných komplikáciách a ich riešení a podpíše písomný informovaný súhlas pacienta s DPV.
Zaradenie pacienta do DPV si vyžaduje špecifickú prípravu, ktorá sa začína hospitalizáciou pacienta v centre DPV.
Na základe antropometrických a laboratórnych vyšetrení (absolútny počet lymfocytov, koncentrácia celkových bielkovín, albumínu, cholinesterázy, transferínu, cholesterolu, C-reaktívneho proteínu) stanovujeme typ a stupeň malnutrície, vypočítavame energetickú potrebu pacienta na základe Harrisovej-Benedictovej rovnice s koreláciou so základným ochorením pacienta, jeho fyzickou aktivitou a telesnou teplotou. Na základe odpadu bielkovín do moču (urea v moči) vypočítavame dusíkovú bilanciu pacienta. Diétny režim zahájime a následne upravujeme s ohľadom na nutričný a somatický deficit (prípravky enterálnej výživy) pacienta, komorbidity (diabetes mellitus, chronické obličkové ochorenie, cholestáza a pod.), stresové faktory. Klinické vyšetrenie a laboratórne parametre kontrolujeme v dvojtýždňových intervaloch (telesná hmotnosť, hladina bielkovín, albumínu, transferínu a lymfocytov) (tab. 5). V prípade prosperovania pacienta ponechávame nastavenú liečbu, v opačnom prípade a pri splnení inklúznych kritérií indikujeme DPV. Pacient indikovaný na DPV podstupuje tréningový program podľa manuálu DPV, v ktorom sa oboznamuje s DPV, prípravou vakov „all in one“ na podávanie do vyživovacieho katétra, starostlivosťou o nutričný katéter, učí sa zásady asepsy, skladovania infúznych roztokov, obsluhovania volumetrickej infúznej pumpy. Počas tréningového procesu lekár centra DPV zasiela do zdravotnej poisťovne tlačivá na schválenie špeciálneho zdravotníckeho materiálu a liečiv, rozpis terapie a použitie pomôcok na jeden týždeň alebo mesiac.
Vzhľadom na potrebu dlhodobého podávania DPV sa k centrálnej kanylácii (v. subclavia, v. jugularis interna, resp. externa) používajú tunelizované Hickmanove alebo Broviakove katétre, alebo pod kožu umiestnené porty, ktoré sú zavádzané v spolupráci s cievnym chirurgom. Hickmanov katéter má vnútornú plochu pokrytú silikónovou alebo polyuretánovou výstelkou, ktorá má nízku trombogenicitu. Má dakrónovú manžetu, ktorá slúži na podkožnú fixáciu katétra a zabraňuje pomnoženiu a prieniku baktérií pozdĺž katétra z kože do podkožia. Pri správnom zavedení by mal byť koniec katétra umiestnený v pravej predsieni, alebo vo v. cava superior. V prípade dočasného podávania sa zavádza periférne zavádzaný centrálny katéter Seldingerovou metódou cez vv. bra- chiales a vv. basilicae, resp. v. axilaris, s umiestnením distálneho konca kavoatriálnom spojení.
Pred demitáciou pacienta do domáceho ošetrenia, pacient a jeden rodinný príslušník, sú preskúšaní z praktických zručností aplikovania „all in one“ vakov v domácom prostredí. Pacient je následne predvolaný na kontroly po týždni, po dvoch týždňoch, po mesiaci a následne každý mesiac až 3 mesiace. Okrem kontroly vnútorného prostredia a nutričného stavu konzultujeme s pacientom problémy pri podávaní DPV.
Záver
Správny management pacientov vyžadujúcich si DPV, vrátane SBS, môže výrazne zlepšiť ich kvalitu života a predísť vzniku komplikácií. Dĺžka podávania DPV je závislá od základnej diagnózy, od východiskového nutričného stavu pacienta a jeho komorbidít. Parenterálny režim u pacienta nastavujeme podľa aktuálnej potreby s možnosťou nielen centrálnej, ale aj periférnej aplikácie parenterálnej výživy, s uprednostňovaním postupného čo najskoršieho prechodu na enterálnu výživu a prirodzený spôsob stravovania. Počas podávania DPV pacienta pravidelne klinicky aj laboratórne kontrolujeme, čím sa snažíme predísť komplikáciám DPV.
V prípade potreby dlhodobého podávania DPV časom okrem metabolických komplikácií môže dôjsť aj k postupnej strate cievneho vstupu, vtedy je vhodné zvažovať alternatívne riešenia.
V neposlednom rade u pacientov s DPV je dôležité sociálne zázemie, resp. zabezpečenie starostlivosti cez ADOS.
O pacientov s potrebou podávania DPV sa musí starať dostatočne odborne spôsobilý personál a v prípade komplikácií musí byť zabezpečená posteľová báza, čo je umožnené centrami DPV s multidisciplinárnou spoluprácou. Problematika DPV je dynamická a potrebuje príliv nových edukovaných lekárov a iných zdravotníckych pracovníkov, ktorí by dokázali reagovať a implementovať aktuálne novinky. Toto si vyžaduje rozšíriť možnosti vzdelávania takýchto pracovníkov v rámci systematického špecializačného/certifikačného ako aj kontinuálneho vzdelávania, pri ktorom by sa mala využívať aj medziodborová spolupráca.
Doručené/Submitted: 31. 10. 2021
Prijaté/Accepted: 17. 1. 2022
doc. MUDr. Katarína Gazdíková, PhD., MHA, MPH, mim. prof.
Katedra všeobecného lekárstva
LF SZU v Bratislave
Limbová 12
833 03 Bratislava
katarina.gazdikova@szu.sk
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené
Literatura
1. Fojtová A, Norek B, Zamborský T et al. Domáca parenterálna výživa – význam a využitie v klinickej praxi. Gastroent Hepatol 2015; 69(5): 449–452. doi: 10.14735/amgh2015449.
2. Pironi L, Boeykens K, Bozzetti F et al. ESPEN guideline on home parenteral nutrition. Clin Nutr 2020; 39(6): 1645–1666. doi: 10.1016/ j.clnu.2020.03.005.
3. Odborné usmernenie organizácie klinickej výživy č. 13163/2006 v znení Odborného usmernenia č. 06242/2008-OZS, vydanom vo Vestníku MZ, čiastka 1–3/2009.
4. NHS National Commissioning Group for highly specialised services. Strategic framework for intestinal failure and home parenteral nutrition services for adults in England 2019. [online]. Available from: http://www.specialisedservices.nhs.uk/library/28/Strategic_Framework_for_Intestinal_Failure_and_Home_Parenteral_Nutrition_Services_for_Adults_in_England_1. pdf.
5. Bozzetti F, Santarpia L, Pironi L et al. The prognosis of incurable cachectic cancer patients on home parenteral nutrition: a multicentre observational study with prospective follow-up of 414 patients. Ann Oncol 2014; 25(2): 487–493. doi: 10.1093/ annonc/mdt549.
6. Dreesen M, Foulon V, Vanhaecht K et al. Guidelines recommendations on care of adult patients receiving home parenteral nutrition: a systematic review of global practices. Clin Nutr 2012; 31(5): 602–608. doi: 10.1016/j.clnu.2012.02.013.
7. Popálená J. Katétrové infekcie u pacientov v programe domácej parenterálnej výživy. [online]. Available from: https://worldmednet.cz.
8. Dreesen M, Foulon V, Spriet I et al. Epidemiology of catheter-related infections in adult patients receiving home parenteral nutrition: a systematic review. Clin Nutr 2013; 32(1): 16–26. doi: 10.1016/j.clnu.2012.08.004.
9. Gahlot R, Nigam C, Kumar V et al. Catheter-related bloodstream infections. Int J Crit Illn Inj Sci 2014; 4(2): 162–167. doi: 10.4103/2229-5151.134184.
10. Pittiruti M, Hamilton H, Biffi, R et al. ESPEN guidelines on parenteral nutrition: central venous catheters. Clin Nutr 2009; 28(4): 365–377. doi: 10.1016/j.clnu.2009.03.015.
11. SSPEV. Manuál a video pre pacientov na DPV. [online]. Available from: https: //sspev.sk/manual-a-video-pre-pacientov-na-dpv/.
12. Robert M, Doneghan P, Graber M et al. Heparin stimulates staphylococcus aureus biofilm formation. Infect Immun 2005; 73(8): 4596–4606. doi: 10.1128/IAI.73.8.4596-4606.2005.
13. Noelting J, Jurewitsch B, Allard J. Non-antibiotic antimicrobial catheter lock solutions in patients on home parenteral nutrition. Nutrients 2018; 10(9): 1165. doi: 10.3390/nu10091165.
14. Blot K, Bergs J, Vogelaers D et al. Prevention of central line-associated bloodstream infections through quality improvement interventions: a systematic review and meta-analysis. Clin Infect Dis 2014; 59(1): 96–105. doi: 10.1093/cid/ciu239.
15. Gabe SM, Culkin A. Abnormal liver function tests in the parenteral nutrition fed patient. Frontline Gastroenterol 2010; 1(2): 98–104. doi: 10.1136/fg.2009.000521.
16. Ondrušová M, Maronová M, Slezáková J. Analýza veľkosti cieľovej populácie pacientov so syndrómom krátkeho čreva. 2019 [online]. Available from: https://www.pharmin.sk.
17. Pironi L, Goulet O, Buchman A et al. Outcome on home parenteral nutrition for benign intestinal failure: a review of the literature and benchmarking with the European prosective survey of ESPEN. Clin Nutr 2012; 31(6): 831–845. doi: 10.1016/j.clnu.2012.05.004.