Přehled nejčastějších kožních nežádoucích účinků biologické léčby u pacientů s idiopatickými střevními záněty – část 1
Michaela Nováková1,2
+ Pracoviště
Éra biologické léčby přinesla zásadní změnu a výrazně zlepšila léčbu Crohnovy nemoci a ulcerózní kolitidy. Biologická léčiva, zejména inhibitory TNFα (tumor nekrotizující faktor α), ovšem mohou také vyvolat široké spektrum kožních projevů. Řadíme mezi ně infuzní reakci a reakci v místě vpichu, xerózu, ekzém, kožní infekce, psoriázu a psoriaziformní dermatitidu, kožní nádory, lupus-like syndrom, vaskulitidu, lichenoidní reakce, granulomatózní reakce, alopecia areata/totalis a vitiligo, erythema exsudativum multiforme, Stevensův-Johnsonův syndrom, toxickou epidermální nekrolýzu (Lyellův syndrom) a dermatomyositidu (tab. 1). Je důležité umět rozpoznat a diagnostikovat tyto projevy jako nežádoucí účinky biologické léčby a dle toho přizpůsobit léčebnou strategii. Některá kožní onemocnění lze léčit pouze lokálně, zatímco jiná vyžadují přerušení/ukončení a změnu biologické léčby [1]. V těžkých a torpidních případech může regrese kožních projevů trvat i několik měsíců po přerušení/ukončení léčby [2]. Inhibitory TNFα mohou vést ke vzniku „paradoxních“ kožních reakcí, které jsou definovány jako nový vznik (80 % případů) nebo exacerbace (20 % případů) dermatóz, pro které se tato léčiva běžně používají [3]. Inhibitory TNFα mají nejvyšší četnost kožních nežádoucích účinků (u 20–25 % pacientů), následované ustekinumabem a blokátory integrinových receptorů [1].
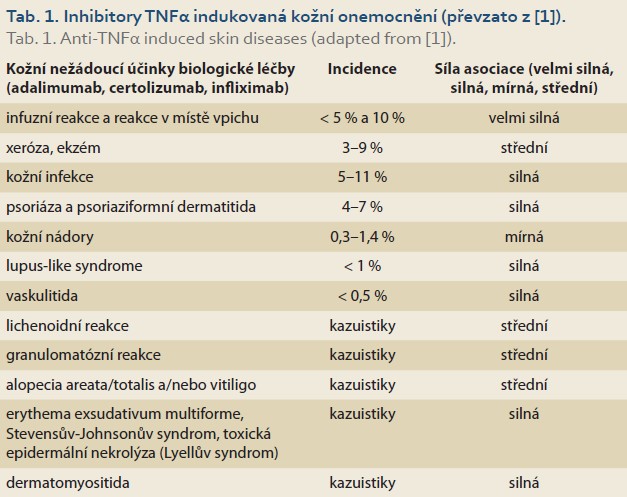
Přehled nejčastějších kožních nežádoucích účinků biologické léčby pacientů s IBD, se kterými se lze v klinické praxi setkat
Infuzní reakce a reakce v místě vpichu
Infuzní reakce
Akutní infuzní reakce byly hlášeny v průběhu minut až 24 hodin od podání infuze infliximabu. Vzácně byly hlášeny i anafylaktické reakce a opožděné hypersenzitivní reakce (objevují se mezi 2 až 14 dny od podání infuze). Projevují se erytémem, kopřivkou, pruritem, návaly horka a sérovou nemocí. Infuzní reakce mohou být mírné, středně závažné a závažné (u 0,1 % infuzí, projevující se hypertenzí, febrilií, hyperemií, tlakem na hrudi s dušností a stridorem). Vyšší riziko infuzních reakcí (2–3×) je při delších časových intervalech mezi podáním infuzí, jelikož nedostatečná hladina infliximabu v séru je příčinou tvorby protilátek proti infliximabu [1,4].
Reakce v místě vpichu
Reakce v místě vpichu (obr. 1) jsou obvykle mírné a projevují se erytémem, otokem, svěděním a bolestí v místě subkutánní aplikace injekce či pera. Jsou častější v prvních měsících léčby, objevují se během 1–24 hodin po aplikaci a příznaky přetrvávají 3–5 dní [1,4].
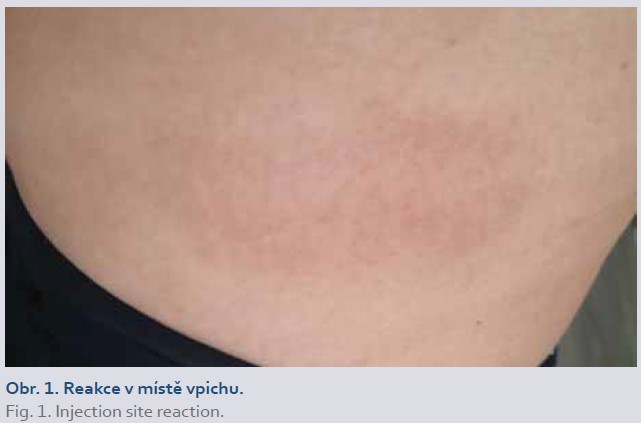
Xeróza, ekzém
Ekzém (obr. 2) se může objevit přibližně u 5–20 % pacientů s IBD léčených inhibitory TNFα. Pozitivní osobní anamnéza atopie ještě zvyšuje toto riziko [1,5]. Při dlouhodobém užívání inhibitorů TNFα se může u pacientů, zejména starších a v zimním období, objevit xeróza (suchá kůže). Xeróza může být předzvěstí ekzému a měla by být zavčas a adekvátně léčena. Inhibitory TNFα mohou indukovat i překryvný syndrom nazývaný „psoriaziformní ekzém“ nebo „psoriaziformní dermatitida“, který se řadí mezi nejčastější kožní nežádoucí účinky biologické léčby. Odlišení ekzému, psoriaziformní dermatitidy a psoriázy může být někdy značně obtížné. V klinickém obraze jsou přítomny typické příznaky (atopické) dermatitidy (xeróza, svědění, bakteriální superinfekce) i psoriázy (silné vrstvy bílých šupin, oranžovo-červené zbarvení) [1]. Histologické vyšetření obdobně odhalí znaky obou onemocnění. Bakteriální superinfekce (obvykle Staphylococcus aureus), která se u psoriázy vyskytuje jen zřídka, je pozoruhodně častá u psoriaziformní dermatitidy [1,5].
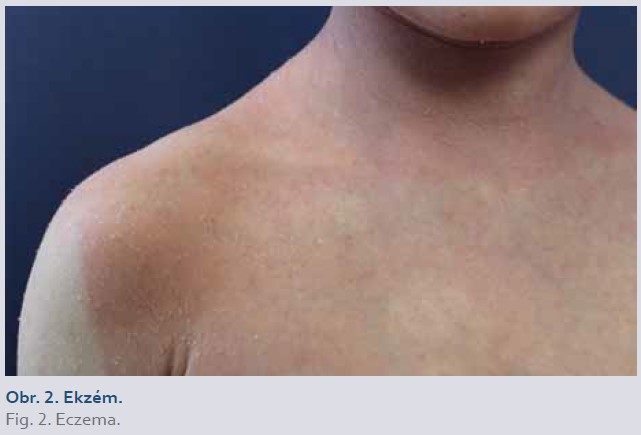
Kožní infekce
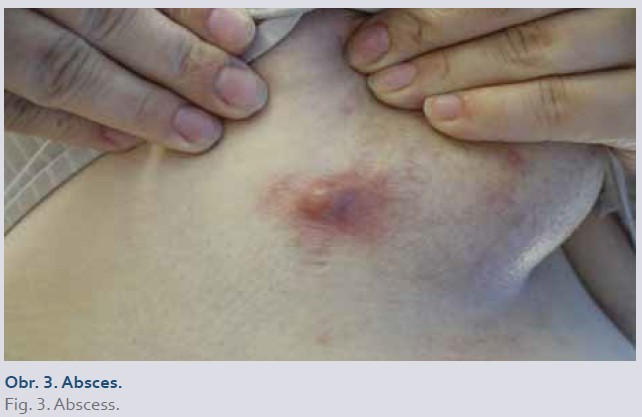
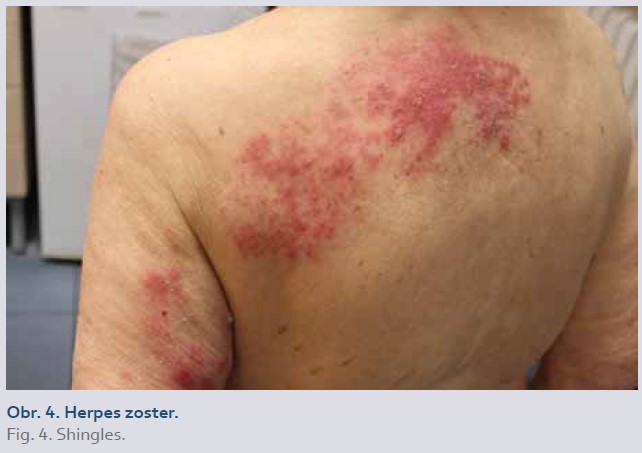
Bakteriální kožní infekce, nejčastěji erysipel, flegmóna (cellulitis) a abscesy (obr. 3, 4), se vyskytují s prevalencí 0,3–3 %. Virové kožní infekce, zejména herpes simplex, herpes zoster a varicella, se vyskytují u 0,7–5 % pacientů [1]. IBD je nezávislým rizikovým faktorem pro vznik herpes zoster [5]. Plísňové kožní infekce, nejčastěji tinea pedis, postihují 0,9–6,9 % pacientů. Zvýšené riziko rozvoje kožních infekcí je u pacientů s konkomitantním podáváním biologické (zejména inhibitory TNFα) a kortikosteroidní terapie [1]. Ustekinumab je obecně spojen s nižším rizikem kožních infekcí ve srovnání s inhibitory TNFα [1,5].
Psoriáza a psoriaziformní dermatitida
Paradoxní psoriáze a psoriaziformní dermatitidě indukované inhibitory TNFα je celosvětově věnována stále větší pozornost. Dle metaanalýzy observačních studií, zahrnujících 24 547 pacientů s IBD léčených inhibitory TNFα, byl výskyt těchto kožních projevů přibližně u 6 % pacientů. Riziko jejich rozvoje významně zvyšuje ženské pohlaví, mladší věk, kouření, ileokolitická forma Crohnovy nemoci a léčba adalimumabem nebo certolizumabem [6]. Jak je uvedeno výše v části o ekzému, u pacientů se může klinický nález do značné míry překrývat („psoriaziformní dermatitida“), což je hlášeno 10× častěji než výskyt paradoxní psoriázy. Ostře ohraničená ložiska krytá bílými až stříbřitými šupinami, nepřítomnost bakteriální superinfekce, mírné či žádné svědění a pomalá odpověď na lokální léčbu svědčí spíše pro diagnózu psoriázy než psoriaziformní dermatitidy. Častým typem paradoxní psoriázy je palmoplantární pustulóza, která je charakterizována výsevem sterilních pustul na živě červené, silně zánětlivé spodině v oblasti dlaní a chodidel [1]. Opakované výsevy pustul vedou ke vzniku chronického erytému s deskvamací a ragádami. Palmoplantární pustulóza se může objevit samostatně nebo navzájem kombinovat s jinými typy psoriázy (chronická ložisková, gutátní, generalizovaná pustulózní psoriáza) nebo s psoriaziformní dermatitidou [2]. Psoriatická alopecie (TIAPA – tumor necrosis factor-alpha inhibitor-associated psoriatic alopecia) se vyskytuje s prevalencí 1,5–5 % a obvykle současně s palmoplantárním postižením (obr. 5). Častější je nejizvící alopecie, vzácně jizvící alopecie [7]. Léčba paradoxní psoriázy vyžaduje trpělivost, protože je často náročná a zdlouhavá [1]. Přechod (switch) na ustekinumab vedl k úplné nebo částečné regresi kožních projevů u 83,1 % pacientů. Přibližně 75,4 % „switchovaných“ pacientů zůstalo v remisi, 4,6 % v parciální remisi a u 20 % došlo k relapsu IBD. Ustekinumab je doporučován jako lék první volby, prokázal účinnost při léčbě paradoxní psoriázy, obzvláště u torpidních případů, a při současné kontrole symptomů IBD [1,8].

Kožní nádory
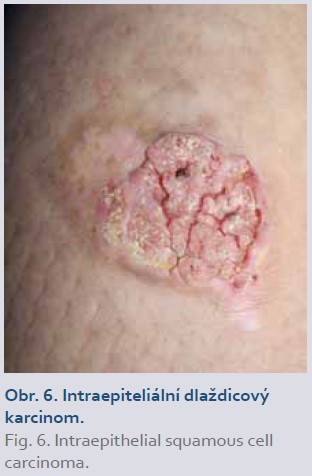
Riziko vzniku melanomu a nemelanomových kožních nádorů je u pacientů s IBD zvýšené. Biologická léčba inhibitory TNFα může toto riziko mírně zvýšit (výsledky jednotlivých studií se rozcházejí, dle některých riziko není zvýšeno), ale nepochybně vyšší riziko je u pacientů léčených imunosupresivy, která mohou způsobit fotosenzitivní reakce (např. thiopuriny) [1,9]. Rizikovými faktory pro vznik kožních nádorů (obr. 6) jsou:
- nadměrná expozice slunečnímu záření;
- nízký fototyp (I, II);
- pozitivní rodinná anamnéza.
U ustekinumabu a blokátorů integrinových receptorů (vedolizumab) nebylo prokázáno zvýšené riziko vzniku kožních nádorů [1].
Lupus-like syndrom
Je známo, že inhibitory TNFα indukují tvorbu autoprotilátek – ANA (20–60 %), anti-dsDNA (15–20 %), antihistonové (15–20 %) a antifosfolipidové protilátky (7–11 %). Lupus-like syndrom vyvolaný inhibitory TNFα je však vzácný (0,19–5,7 % u infliximabu a 0,1–0,6 % u adalimumabu) a bez klinické manifestace bychom se měli vyhnout jejich systematickému sledování [1]. Rizikovými faktory pro vznik lupus-like syndromu jsou [1,10,11]:
- ženské pohlaví;
- zahájení léčby ve vyšším věku.
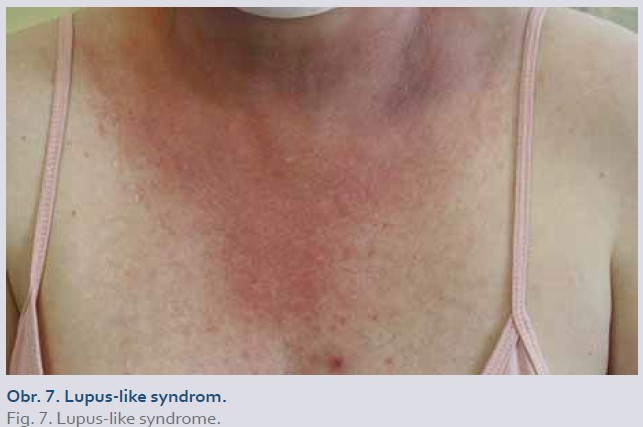
Diagnóza se stanoví na základě časového vztahu mezi symptomy a zahájením léčby inhibitory TNFα a jejich regresí po ukončení léčby, přítomnosti autoprotilátek (ANA, anti-dsDNA) a alespoň jednoho doplňujícího kritéria – např. kožní projevy podobné lupusu (motýlovitý a makulopapulózní exantém), bolest kloubů, horečka, únava a serozitida [1,4]. Kožní projevy lupus-like syndromu (obr. 7) obvykle regredují během pár týdnů po ukončení biologické léčby. Lupus-like syndrom vyvolaný ustekinumabem a vedolizumabem je vzácný (jsou publikovány pouze jednotlivé kazuistiky) [1].
Vaskulitida
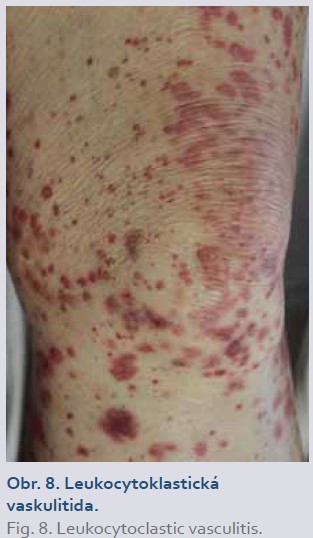
Leukocytoklastická vaskulitida (obr. 8), obvykle charakterizovaná palpovatelnými purpurovými plaky na dolních končetinách, se vyskytuje u 0,5 % pacientů s IBD léčených inhibitory TNFα. Erythema elevatum diutinum je vzácná forma kožní vaskulitidy, která se projevuje symetrickými červenými či červenofialovými tuhými noduly na akrálních částech těla a nad extenzorovými oblastmi kloubů. Může být doprovázena horečkou, artralgiemi a očními komplikacemi (uveitida/skleritida) [1].
Lichenoidní reakce
Bylo popsáno více než 120 případů lichenoidní reakce (dermatitidy) po inhibitorech TNFα (obr. 9). Rozlišujeme tři formy:
1. lichen planus s typickými projevy – purpurické, ploché, polygonální papuly s bělavou kresbou na povrchu;
2. lichen s nespecifickými eflorescencemi (makuly nebo papuly);
3. klinicky psoriáza, ale histologicky s lichenoidními rysy.
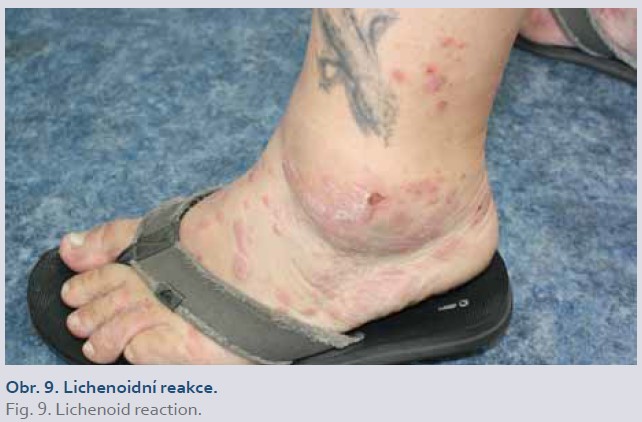
Klinická manifestace může být různá, ale histologický nález lichenoidní „interface“ dermatitidy nám potvrzuje výše zmiňovanou diagnózu [1,5]. U pacientů léčených inhibitory TNFα se vyskytly i formy lichen planus pigmentosus, lichen planopilaris, který může vést k nevratné ztrátě vlasů (jizvící alopecie) [1,12]. U ustekinumabu a blokátoru integrinového receptoru (vedolizumab) nebyly lichenoidní reakce popsány [1].
Granulomatózní reakce
Granulomatózní reakce jsou heterogenní skupinou chronických zánětlivých kožních onemocnění, které mohou být vyvolány i léčbou inhibitory TNF [1,13]. Řadíme mezi ně:
- granuloma annulare (obr. 10);
- léky indukovanou sarkoidózu (DISR – drug-induced sarcoidosis-like reaction);
- intersticiální granulomatózní dermatitidu.
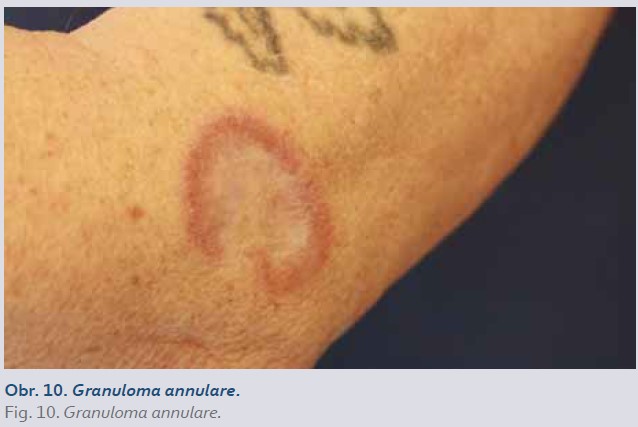
Granuloma annulare se vyskytuje především v diseminované formě charakterizované anulárními (prstencovitými) ložisky červenorůžové barvy s hmatným lemem. Léky indukovaná sarkoidóza se manifestuje červenohnědými papulami, které vznikají přednostně ve starých jizvách (tzv. sarkoid v jizvě). U intersticiální granulomatózní dermatitidy nacházíme erytematózní plaky v oblasti trupu a končetin [1,14].
Alopecia areata/totalis a vitiligo
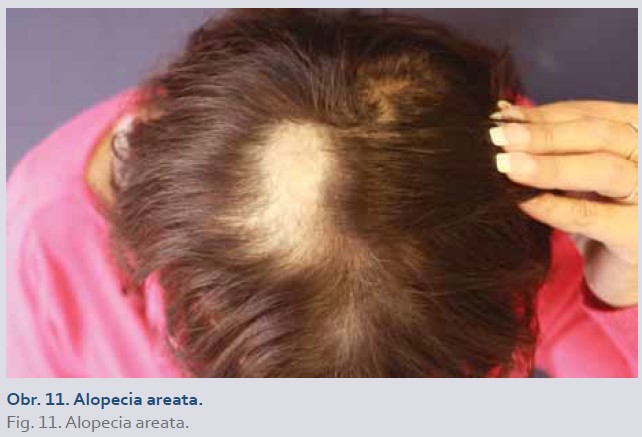
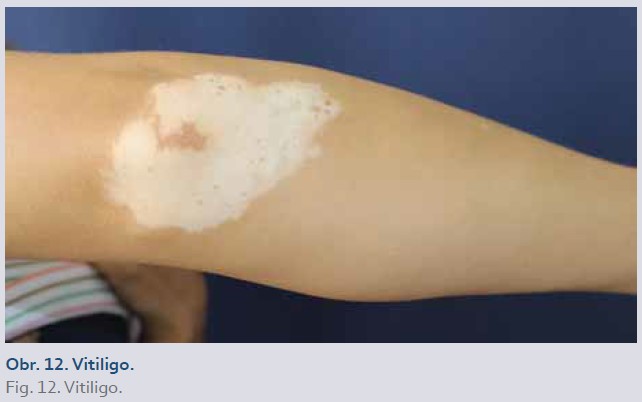
Bylo popsáno několik případů nově vzniklé alopecie areata/totalis a vitiliga u pacientů s IBD léčených inhibitory TNFα (obr. 11, 12). Vitiligo se projevuje depigmentovanými ložisky kůže. Alopecia areata je charakterizována vznikem ostře ohraničených bezvlasých ložisek nejčastěji ve kštici, která mohou vést až k úplné ztrátě vlasů (alopecia totalis).
Erythema exsudativum multiforme (EEM), Stevensův--Johnsonův syndrom (SJS), toxická epidermální nekrolýza (Lyellův syndrom)
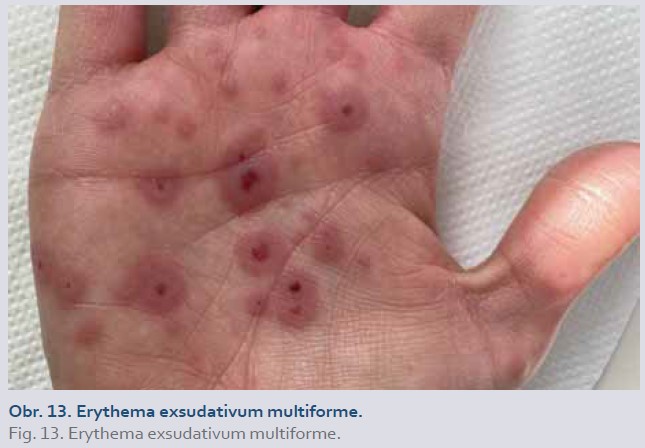
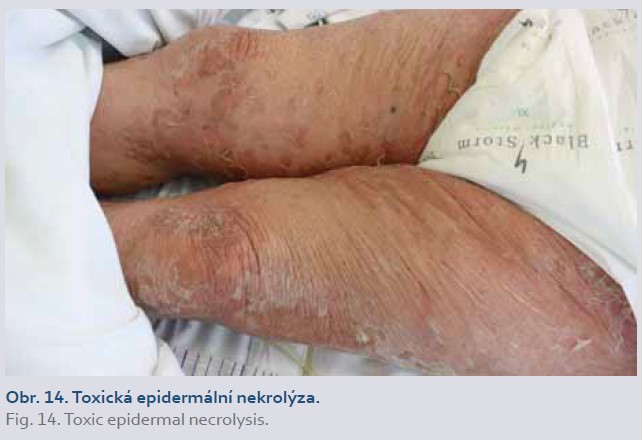
U pacientů léčených inhibitory TNFα byly vzácně popsány jednotlivé případy těchto konkrétních diagnóz, které řadíme mezi závažné kožní nežádoucí reakce (SCAR – severe cutaneous adverse reactions) [1,15]. Pro EEM (obr. 13) jsou charakteristické typické terčovité léze (erytematózní makulopapuly) primárně na extenzorových plochách končetin (dlaně a chodidla), případně i na sliznicích. SJS postihuje < 10 % tělesného povrchu (BSA – body surface area), zatímco u TEN (obr. 14) je postiženo > 30 % BSA, postižení mezi 10 a 30 % BSA označujeme jako SJS/TEN „overlap“ syndrom. Postižení sliznic se vyskytuje v 90 % případů, bývá nejméně na dvou různých místech. Léky jsou nejčastějším spouštěcím faktorem těchto diagnóz, následované infekcemi (virové – herpes simplex virus) [1,16].
Dermatomyositida
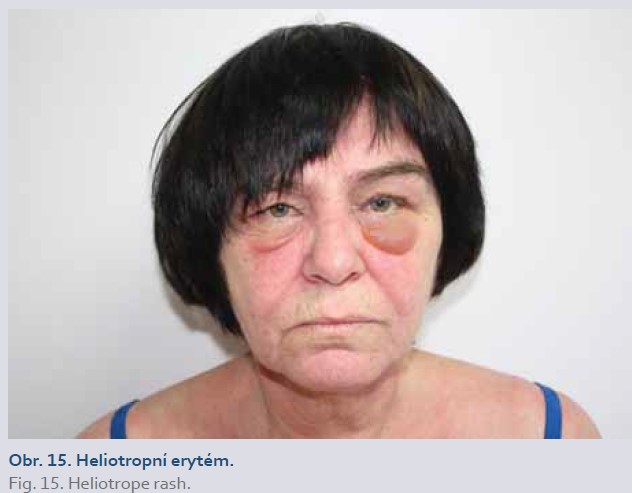
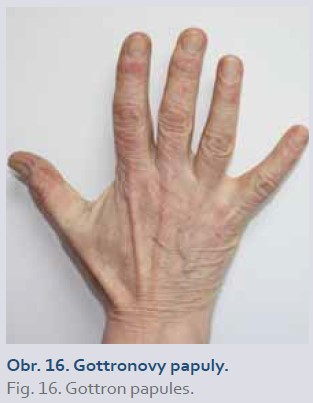
Dermatomyositida (DM) a polymyositida (PM) jsou idiopatické zánětlivé myopatie postihující jedince všech věkových kategorií. Pro DM je charakteristické systémové postižení (symetrické svalové slabosti, únava, horečka, artralgie, dysfagie, dysfonie) a typické kožní projevy – červenofialové zbarvení očních víček, často spojené s periorbitálním edémem (heliotropní erytém, obr. 15) a lehce se šupící papuly až plaky nafialovělé barvy nejčastěji nad metakarpofalangeálními a interfalangeálními klouby (Gottronovy papuly, obr. 16) [1,17]. U léčby ustekinumabem nebyl pozorován rozvoj DM [1].
Závěr
Mukokutánní manifestace IBD a kožní nežádoucí účinky biologické léčby jsou relativně časté a mohou mít dopad i na kvalitu života pacientů [3,7,18]. Kožní projevy indukované inhibitory TNFα jsou velmi různorodé. Nezávislé prediktivní faktory pro jejich rozvoj jsou: ženské pohlaví, kouření, vyšší BMI, Crohnova nemoc, rodinná či osobní anamnéza kožního zánětlivého onemocnění, léčba adalimumabem [3]. Jejich včasné rozpoznání je důležité pro volbu terapeutického postupu [1]. Mezioborová spolupráce mezi gastroenterology a dermatology při jejich diagnostice a léčbě je nezbytná [3].
Fotografie
Archiv Dermatovenerologické kliniky 2. LF UK a FN Bulovka.
Tento článek vznikl s podporou společnosti Janssen-Cilag s. r. o.
EM-122860, datum přípravy: leden 2023.
MUDr. Michaela Nováková
Dermatovenerologická klinika
2. LF UK a FN Bulovka
Budínova 67/2
180 81 Praha 8
michaela.novakova@bulovka.cz
Literatura
1. Lambert JLW, De Schepper S, Speeckaert R. Cutaneous Manifestations in Biological-Treated Inflammatory Bowel Disease Patients: A Narrative Review. J Clin Med 2021; 10(5): 1040. doi: 10.3390/jcm10051040.
2. Ungureanu L, Cosgarea R, Alexandru Badea M et al. Cutaneous manifestations in inflammatory bowel disease (Review). Exp Ther Med 2020; 20(1): 31–37. doi: 10.3892/etm.2019.8321.
3. Antonelli E, Bassotti G, Tramontana M et al. Dermatological Manifestations in Inflammatory Bowel Diseases. J Clin Med 2021; 10(2): 364. doi: 10.3390/jcm10020364.
4. Pasadyn SR, Knabel D, Fernandez AP et al. Cutaneous adverse effects of biologic medications. Cleve Clin J Med 2020; 87(5): 288–299. doi: 10.3949/ccjm.87a.19119.
5. Lee J, Lemons N, Lorenze A et al. Management of cutaneous side effects of inflammatory bowel disease therapy: A dermatologic viewpoint. J Gastroenterol Hepatol 2021; 36(12): 3278–3285. doi: 10.1111/jgh.15570.
6. Xie W, Xiao S, Huang H et al. Incidence of and Risk Factors for Paradoxical Psoriasis or Psoriasiform Lesions in Inflammatory Bowel Disease Patients Receiving Anti-TNF Therapy: Systematic Review With Meta-Analysis. Front Immunol 2022; 13: 847160. doi: 10.3389/fimmu.2022.847160.
7. Jeong KM, Seo JY, Kim A et al. Tumor Necrosis Factor-Alpha Inhibitor-Associated Psoriatic Alopecia in a Patient with Ulcerative Colitis: A Case Report and Review of the Literature. Ann Dermatol 2021; 33(1): 82–85. doi: 10.5021/ad.2021.33.1.82.
8. Revankar R, Patel H, Rojas M et al. Systematic review of TNFα-induced paradoxical psoriasis: Treatment outcomes of switching to alternative biologic therapies in inflammatory bowel disease patients. J Dermatolog Treat 2022: 1–4. doi: 10.1080/09546634.2022.2133533.
9. Giagkou E, Saridi M, Albani E et al. Dermal Lesions and Skin Cancer in Patients with Inflammatory Bowel Disease Receiving Immunosuppressive Therapy. Asian Pac J Cancer Prev 2018; 19(10): 2845–2851. doi: 10.22034/APJCP.2018.19.10.2845.
10. Macaluso FS, Sapienza C, Ventimiglia M et al. Lupus-like reactions in patients with inflammatory bowel disease treated with anti-TNFs are insidious adverse events: data from a large single-center cohort. Scand J Gastroenterol 2019; 54(9): 1102–1106. doi: 10.1080/00365521.2019.1663260.
11. Picardo S, So K, Venugopal K. Anti-TNF-induced lupus in patients with inflammatory bowel disease. JGH Open 2019; 4(3): 507–510. doi: 10.1002/jgh3.12291.
12. McPhie ML, Wang A, Molin S et al. Lichen planopilaris induced by infliximab: A case report. SAGE Open Med Case Rep 2020; 8: 2050313X20901967. doi: 10.1177/2050313X20901967.
13. Garcovich S, De Simone C, Genovese G et al. Paradoxical Skin Reactions to Biologics in Patients With Rheumatologic Disorders. Front Pharmacol 2019; 10: 282. doi: 10.3389/fphar.2019.00282.
14. Miedema J, Nunes H. Drug-induced sarcoidosis-like reactions. Curr Opin Pulm Med 2021; 27(5): 439–447. doi: 10.1097/MCP.0000000000000800.
15. Hertl M. Severe Cutaneous Adverse Drug Reactions. In: Plewig G, French L, Ruzicka T et al (eds). Braun-Falco’s Dermatology. Berlin, Heidelberg: Springer 2022. Dostupné z: https: //doi.org/10.1007/978-3-662-63709-8_36.
16. Toledo-Martinez JF, Galdamez-Carcamo EV, Somoza-Cano FJ et al. Recurrent Steven-Johnson/Toxic Epidermal Necrolysis Overlap Syndrome. Cureus 2022; 14(1): e21364. doi: 10.7759/cureus.21364.
17. Qudsiya Z, Waseem M. Dermatomyositis. 2022. In: StatPearls [online]. Treasure Island (FL): StatPearls Publishing 2022.
18. Keller R, Mazurak N, Fantasia L et al. Quality of life in inflammatory bowel diseases: it is not all about the bowel. Intest Res 2021; 19(1): 45–52. doi: 10.5217/ir.2019.00135.