Kortikorezistence v léčbě idiopatických střevních zánětů I. Teoretické podklady
Vladimír Zbořil Orcid.org 1, Lucie Prokopová Orcid.org 1, Renata Gaillyová Orcid.org 2, Barbora Ravčuková Orcid.org , Jana Řádková Orcid.org , Ladislava Bartošová Orcid.org 3, Milan Bartoš Orcid.org , Petr Dítě Orcid.org 4,5
+ Pracoviště
Souhrn
Kortikosteroidní rezistence představuje závažný léčebný, ale také diagnostický problém u řady chorob, mimo jiné také u idiopatických střevních zánětů. Autoři shrnují dosavadní poznatky o této problematice v gastroenterologické literatuře a docházejí k závěru, že existují s největší pravděpodobností dva typu kortikorezistence. Klinicky definovaná kortikorezistence se opírá o empirické poznatky a neexistuje na ni v odborné literatuře jednotný pohled. Do protiváhy k ní by bylo možné postavit kortikorezistenci definovanou geneticky. V gastroenterologické literatuře však dosud tato definice podána nebyla. Autoři se proto s podporou grantových projektů zaměřili na vypracování a uvedení do klinické praxe právě geneticky definované kortikorezistence u nemocných s idiopatickými střevními záněty. Na základě vlastních zkušeností navrhujeme rozdělení kortikorezistencí na tzv. pravé (geneticky, resp. imunogeneticky definované) a nepravé, které jsou důsledkem chyb v použití kortikosteroidů, komplikací léčby a přidružených chorob. K rizikům vzniku nepravé kortikorezistence patří snížení sérových proteinů, snížení hladiny zinku, oportunní infekce a superinfekce v průběhu kortikosteroidní léčby, pokles sérového IgG a především nevhodná dávkovací schémata kortikosteroidů.
Klíčová slova: idiopatické střevní záněty - Crohnova nemoc - ulcerózní kolitida - glukokortikosteroidy - kortikorezistence.
ÚVOD
Kortikosteroidní rezistence představuje závažný léčebný problém u nemocných s idiopatickými střevními záněty. Navzdory novým léčebným postupům, zejména biologické terapii, zůstávají glukokortikosteroidy (GCS) stále základem terapie. Literatura uvádí, že v průběhu prvních pěti let onemocnění tuto léčbu absolvuje více než 87 % nemocných(1,2). Výskyt kortikorezistence je však uváděn různými autory od 10 % až dokonce do 39 %. Je proto nanejvýš potřebné se problémem kortikorezistence zabývat.
Na úvod k problematice kortikorezistence je třeba shrnout některá základní fakta o principech léčby kortikosteroidy u idiopatických střevních zánětů (ISZ).
ÚLOHA KORTIKOSTEROIDŮ V LÉČBĚ IBD
GCS působí na mimobuněčné a buněčné úrovni směsí protizánětlivých a imunomodulačních, převážně imunosupresivních účinků. Mimo pozitivních vlivů na střevní propustnost a kolonickou stimulaci absorpce vody a sodíku jsou ostatní systémové účinky na ISZ nežádoucí. K realizaci působení GCS na subcelulární úrovni je nutná přítomnost zinku. Protizánětlivé účinky jsou jednak okamžité - dominující za 6 hodin po injekčním podání GCS, které však do 24 hodin odeznívají a souvisí s kvantitativními změnami cirkulujících leukocytů, jednak pozdní. Ve vysokých dávkách působí GCS na B-lymfocyty a mohou způsobovat pokles tvorby IgA a IgG za 2-3 týdny léčby. Později nastupující, ale dlouhodobé protizánětlivé účinky se uplatňují vlivem na T-lymfocyty, především na helperové buňky a podstatně méně na supresorové, avšak NK-buňky zůstávající neovlivněny. Nevýhodou léčby GCS je snížení obranné imunitní reakce především tlumením funkčních schopností monocytů a makrofágů. Reakce abnormních lymfocytů se výrazně liší od zdravých, což je třeba zohlednit u přidružených onemocnění(3-5).
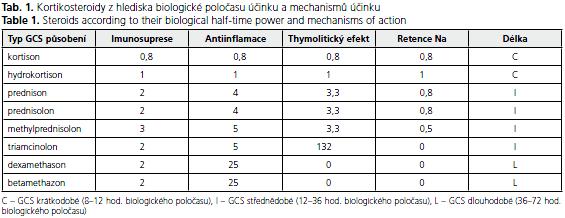
Jednotlivé GCS se liší protizánětlivými, imunosupresivními, ale i dalšími účinky, jako jsou thymolytické a natriumretenční, což je velmi důležité z hlediska jejich výběru při terapii(6-10). Přehled podává následující tabulka 1.
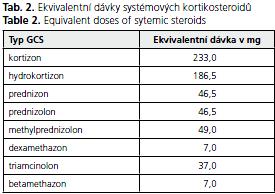
Tabulka 1 záměrně neuvádí tzv. ekvivalentní dávku v mg, nebo» ta je vytvářena s ohledem na systémové účinky GCS pro předpokládaný přechod z jednoho typu GCS na jiný, avšak nezahrnuje běžně srovnání účinků imunosupresivních a protizánětlivých. K těm je třeba provést samostatnou kalkulaci. Základní poměr tzv. ekvivalentních dávek GCS uvádíme v tabulce 2.
Vedle klasických systémových kortikosteroidů jsou v léčbě IBD k dispozici tzv. topické kortikosteroidy. Jejich výhodou je minimální vedlejší systémový účinek, který je například u budesonidu zajištěn mechanismem tzv. first pass effectu, kdy při prvním průchodu játry se mění 90 % účinné látky na systémově neaktivní metabolity. Budesonid je k dispozici také ve formě rektálních nálevů, jejichž účinnost je hodnocena jako srovnatelná s lokálně aplikovanými aminosalicyláty. Hlavní indikací orální formy budesonidu je Crohnova nemoc (CN), zatímco při ulcerózní kolitidě (UC) se uplatní lokální forma nálevů.
Léčba systémovými steroidy je zahajována obvykle v dávce 0,5-1,0 mg/kg/den s postupným sestupem k tzv. dávkám udržovacím, jež se pohybují pod hranicí 20 mg/den. Není rozhodně doporučováno iniciační podávání nízkých nebo středních dávek, což vede k oddálení nástupu efektivity léčby, jak prokázala již v roce 1962 Baronová(11).
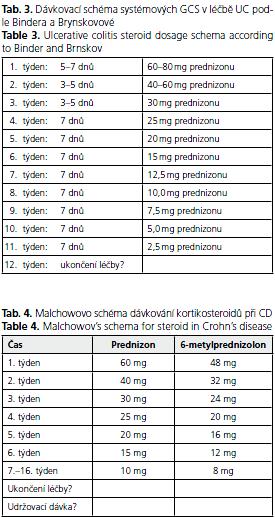
Další snižování iniciační dávky systémového kortikosteroidu je obvykle realizováno dle schématu vypracovaného Binderem a Brynskovovou pro léčbu UC(12), které uvádíme v tabulce 3.
Pro použití systémového kortikosteroidu u CN je vypracováno aplikační schéma dle Malchowa z roku 1984(13), které citujeme v tabulce 4.
Při realizaci léčby kortikosteroidy narážíme v klinické praxi na dva specifické problémy, které se částečně překrývají - totiž na kortikodependenci a kortikorezistenci.
KORTIKODEPENDENCE
Lukáš a spol.(1) definuje kortikodependenci jako stav, kdy při snížení dávky GCS dochází k manifestaci choroby, což ve svém důsledku znemožňuje GCS postupně vysadit. Přitom víme, že GCS nemají (mimo budesonidu v ileocekální lokalizaci) prokazatelně pozitivní vliv na prevenci relapsů ISZ. Tato definice je klinicky snadno aplikovatelná, ovšem klade před nás několik otázek. Jak hodnotit manifestaci choroby - podle aktivity? Jaká dávka GCS při snižování je hraniční pro hodnocení kortikoidní dependence? Ve světové literatuře nacházíme několik možností hodnocení, ale jejich definice nejsou jednotné. Většina autorů považuje za hraniční dávku GCS 10-20 mg prednizonu/prednizolonu na den, např. Reinisch(14) či Munkholmová(15). V publikaci Allana et al. podávají definici kortikoidní dependence Binder a Brynskovová(12) pouze nepřímo. Sami se domníváme, že je třeba tento problém hodnotit ze dvou hledisek:
1. Jestliže mimo výjimečné efektivity budesonidu na prevenci relapsů CN v ileocekální krajině není důkaz pro pozitivní roli GCS v prevenci relapsů ISZ, pak tedy nemožnost vysadit jakoukoliv dávku GCS, aniž by se neaktivovala CN nebo UC, je projevem kortikodependence.
2. Pokud nelze GCS z důvodů rizika reaktivace či relapsu ISZ vysadit, je důležité, na jakou dávku můžeme bezpečně systémový GCS snížit. Za tzv. bezpečnou dávku prednizonu/prednizolonu, tedy dávku, při jejíž dlouhodobé aplikaci jsou vedlejší účinky terapie minimální až klinicky neprokazatelné, se u dospělých s průměrnou váhou kolem 70 kg považuje 7,5 mg prednizonu/prednizolonu na den, případně ekvivalentní dávka dalších GCS. Tuto dávku podle literárních referencí a našich zkušeností lze ponechat řádově měsíce bez obav ze zásadních vedlejších účinků. Zároveň však mějme na paměti, že touto léčbu pouze "kryjeme" aktivitu ISZ, ale neřešíme otázku dalšího vývoje nemoci. Proto se musíme nadále pokoušet GCS eliminovat z léčby nebo je nahradit. Jestliže bychom nemohli dávku prednizonu/prednizolonu snížit ke zmíněné hranici 7,5 mg/den, pak je to signál pro změnu léčebné strategie, nebo» dlouhodobou léčbou středními nebo dokonce vyššími dávkami GCS kumulujeme vedlejší účinky této terapie a prognózu choroby opět neřešíme.
Tuto definici nabízíme k úvaze především z praktického hlediska na základě vlastních, dosud nepublikovaných zkušeností, nebo» se domníváme, že nutí gastroenterologa k aktivnímu přístupu k terapii a chrání pacienta před zbytečnými vedlejšími účinky GCS. Za kortikodependenci však nepovažujme aktivaci choroby nebo relaps či recidivu poté, co již byla ukončena úspěšná terapie GCS až do úplného vysazení.
Z praktického hlediska považujeme ještě za vhodné upozornit, že ne každé zhoršení příznaků ISZ v průběhu sestupu a eliminace GCS musí znamenat kortikodependenci. Může se jednat o exogenní či endogenní infekce, které průběh základní nemoci komplikují, ale se samotným efektem GCS nesouvisí. Terapeutická řešení kortikodependence s využitím farmakoterapie počínaje aminosalicyláty a biologickou terapií konče podává přehledně práce Pannacciona(16) z roku 2008.
KORTIKOREZISTENCE
S definováním kortikorezistence je stejný problém jako s kortikodependencí, klinická aplikace je však ještě obtížnější.
Kortikorezistenci lze totiž definovat dvojím způsobem: 1. imunologicky, 2. klinicky. Bohužel mezi oběma definicemi nelze v současné době stanovit jasné pojítko, jinak řečeno, jen velmi obtížně lze ověřit (v oblasti experimentální preklinické medicíny), že definice klinická má imunologicky ověřitelný podklad.
Imunologická definice kortikorezistence
Podklad má zřejmě v problematice vazby GCS na tkáňové receptory. Linder(17) se domnívá, že podkladem kortikorezistence jsou abnormality receptorového genu a mRNA u tzv. primární kortizolové rezistence. Hurley(18) prokazuje možnou familiární vazbu steroidní rezistence, Brufsky(19) prokázal u jedinců s kortikorezistencí receptorovou mutaci. Lamberts(20) se již zajímá o klinickou vazbu receptorové rezistence a lze pouze litovat, že při exaktním ověření receptorové charakteristiky monocytů a kortikorezistence postoupily například alergologové v klinice bronchiálního astmatu(21) dále než současná gastroenterologie. Nicméně i zde se vyskytují v posledním desetiletí studie, které se zabývají genovými polymorfismy z pohledu efektivity kortikosteroidní léčby u ISZ(22-24). V naší literatuře posledních let podává přehled faktorů, za nimiž se může skrývat kortikorezistence, práce Matouše(25). Autor v ní zdůrazňuje tři základní faktory jejího vzniku: přítomnost MDR1 (multidrug resistance gene)(22,26), abnormality GCS receptoru a kolísající aktivitu NF-κB. Prací, které by se zabývaly průkazem abnormální aktivity GCS receptorů u ISZ, je ovšem velmi málo(23,24,27), podobně jako v případě alterace NF-κB(28).
Klinická definice kortikorezistence
V gastroenterologii se v současné době opíráme o empirické zkušenosti průběhu léčby GCS u konkretních nemocných.
Lukáš a spol.(1) definuje kortikorezistenci jako stav, kdy léčba GCS není schopna remisi IBD navodit, nebo je nutno podávat více než 30 mg prednizonu/prednizolonu denně. V literatuře je často používána definice podle Modiglianiho z roku 1990(29):
Kortikorezistence v terapii ISZ je klinický stav, kdy po navození remise dochází při snižování dávky GCS k relapsu neragujícímu na jejich opětovné navýšení o 50 %.
Samozřejmě i k této definici lze vyslovit řadu výhrad, nicméně ji zde nabízíme jako relativně přesně vymezenou a ponecháváme na volbě odborníků, zda se jim osvědčí v praxi. Přinejmenším upřesní jinak dosti vágní vymezení tohoto termínu.
Výskyt kortikorezistence je uváděn sumárně Lukášem a spol.(1) na hranici 10-15 %. Studie Munkholmové uvádí pro první ataku CN kortikorezistenci kolem 20 %(15), ale Summers(30) ji hodnotil až jako 39 %. Rozpor zřejmě pochází z kritérií hodnocení kortikorezistence, jak byla výše rozebrána. Po první atace UC odhaduje Kjeldsen(31) kortikorezistenci na 11-17 % léčených. Novější práce jako Faubinova(32) a Creedova(33) dospívají k podobným závěrům.
Možné příčiny kortikorezistence
Naprostá většina prací se soustředí na otázku dalšího postupu léčby při známkách kortikorezistence(33) a jen okrajově registruje situaci, v níž tento jen nastal. Vzhledem k jeho závažnosti z hlediska další léčby a prognózy nemoci jsme se zaměřili na rozbor příčin a považujeme za vhodné zde ve zkratce prezentovat výsledky naší studie.
Vycházeli jsme ze skutečnosti, že u části pacientů skutečně existuje imunologicky definovaná kortikorezistence, která spočívá v poruše vazby GCS na jeho cílový receptor. Tyto stavy jsme označili jako pravé kortikorezistence. Domníváme se, že vedle nich však existují kortikorezistence nepravé. Jejich podstatou je chybné použití GCS, komplikace léčby GCS a chybná interpretace komplikujících onemocnění jako známek rezistence na nasazení GCS.
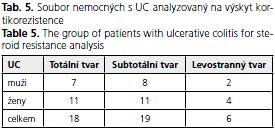
Vyšetřovali jsme celkem soubor 43 pacientů s UC, 24 mužů a 19 žen, 18 s totální kolitidou a 25 se subtotální nebo levostrannou formou UC (tab. 5).
Kortikorezistence pravé byly prokázány v 15-19 případech ze souboru 43 pacientů. Jednalo se o nemocné, u nichž jsme nenalezli žádnou možnou příčinu kortikorezistence mimo výrazně sníženého imunoregulačního indexu CD4/CD8 - ve čtyřech případech. Interpretace tohoto nálezu je ovšem problematická a přesahuje rámec probírané problematiky.
Jako kortikorezistence nepravé jsme označili 28 případů, v nichž byla prokazatelná příčina vzniklého stavu, která byla odstranitelná nebo léčebně ovlivnitelná:
Ve 24 případech léčby GCS jsme prokázali chyby v léčebné strategii GCS, jako je poddávkování, střední dávka dlouhodobě podávaná bez dávky iniciální apod. Ve většině případů při zpětné analýze nebylo možno ani o nějakém schématu či obecné strategii léčby GCS hovořit.
U 16 pacientů byla významně snížena hladina sérového Zn, o němž je známo, že je nezbytný pro vazbu GCS na receptor(25,34).
Ve 28 případech byla konstatována nepříznivá nutriční situace, z nichž 13 pacientů mělo snížené hladiny sérových proteinů. Také o této skutečnosti je známo z farmakokinetiky GCS, že snížení hladiny vazebných proteinů zvyšuje volnou GCS frakci, a tím vedlejší účinky a současně klesá frakce vázaná a její transport k cílovým receptorům.
V 5 případech jsme zaregistrovali snížení hladiny IgG ve 3.-4. týdnu léčby GCS s poklesem pod hranici normy. Tento nález lze zdůvodnit v souvislosti s přidružením oportunních infekcí a superinfekcí zažívacího traktu, a tím druhotně selhání léčby GCS. Druhotně proto, že příčinou zhoršení nebo snížené reaktivity na GCS není rezistence na ně, ale přidružená infekce s reaktivací zánětu.
Diskutovatelné jsou i další nálezy jako problém průkazu anti-gliadinových protilátek ve třídě IgE nebo otázka chronobiologického podávání GCS(34). Kortikorezistenci se nedoporučuje "zvládat" výrazným a dlouhodobým navyšováním dávek GCS, zejména ne extrémně vysokým dávkováním, jehož obecně diskutovaná efektivita je zřejmě limitována funkční receptorovou kapacitou(10,23,27).
Použité zkratky
ISZ - idiopatické střevní záněty
CN - Crohnova nemoc
UC - ulcerózní kolitida
GCS - glukokortikosteroidy
MDR1 - multidrug resistance gene
NF-κB - nukleární faktor kappa B
Práce byla podpořena grantovými projektem IGA NR/8071-3 a IGA NR 9342-3/2007.
LITERATURA
- 1. Lukáš M. Medikamentózní terapie idiopatických střevních zánětů. In Lukáš M. Idiopatické střevní záněty: nejistoty, současné znalosti a klinický přístup. Praha: Galén 1998: 254.
- 2. Binder V, Brynskov J. Corticosteroids. In: Allan RN. Inflammatory Bowel Disease. New York, Edinburgh, London, Madrid, Melbourne, San Francisco, Tokyo: Churchill Livingstone 1997: 503-511.
- 3. Cohen JJ. Lymphocyte death induced by glucocorticoids. In Antiinflammatory steroid action. Basis and clinical aspects (Eds. Schleimer RP, Claman HN, Oronsky AL). San Diego: Academic Press Inc. 1989: 110-131.
- 4. Claman HN. Glucocorticosteroids. I. Antiinflammatory mechanism. Hosp Pract 1983; 18: 123.
- 5. Besedovsky J, Del Rey A, Sorkin E, Dinarello C. Immunoregulatory feedback between IL-1 and glucocorticoid hormones. Science 1986; 233: 652-654.
- 6. Winkelstein A. Imunosupresivní léčba. In Základní a klinická imunologie (Eds. Stites DP, Terr AI.). Praha: Victoria Publishing a.s., 1994: 690.
- 7. Cupps TR, Fauci AS: Corticosteroid-mediated immunoregulation in man. Immunol Rev 1982; 65:133.
- 8. Lefer AM. Mechanismus účinku glukortikoidů v šoku - stabilizace buněčných a lysozomálních membrán. Sborník symposia Upojhn CS Kortikosteroidy v neodkladné péči, 1986: 27-28.
- 9. Rachmilewitz D, Eliakim R, Simon P, Ligumsky M, Karmeli F. Cytokines and platelet-activating factor in human inflammed colonic mucosa. Agents Actions 1992;36: C32-C36.
- 10. Muller M, Renkawitz R: The glucocorticoid receptor. Biochem Biophys Acta 1991; 1088: 171-182.
- 11. Baron JH, Connell AM, Kanaghinis TG, Lennard- Jones JE, Avery Jones FA. Out-patient treatment of ulcerative colitis. Comparsion between three doses of oral prednisolone. Br Med J 1962; 2: 441-443.
- 12. Binder V, Brynskov J. Corticosteroids. In Inflammatory Bowel Disease. New York, Edinburgh, London, Madrid, Malbourne, San Francisco, Tokyo: Churchill- Livingstone 1997; 503-511.
- 13. Malchow H, Ewe K, Brandes JW. European cooperative Crohn’s disease study: results of drug treatment. Gastroenterology 1984; 86: 249-266.
- 14. Reinisch W, Gasche C, Wyatt J, moser G, Lochs H, Vogelsang H, Gang A. Steroid dependence in Crohn’s disease. Lancet 1995; 354: 859 (letter).
- 15. Munkholm P, Langholz E, Davidsen M, Binder V. Frequency of glucocorticoid resistance and dependency in Crohn’s disease. Gut 1994; 35: 360-362.
- 16. Panaccione R, Rutgeerts P, Sandborn WJ, et al. Review artikle: treatment algorithms to maximize remission and minimize corticosteroid dependence in patients with inflammatory bowel disease. Aliment Pharmacol Ther 2008; 28: 674-688.
- 17. Linder MJ, Thompson EB. Abnormal glucocorticoid receptor gene and mRNA in primary cortisol resistance. J Steroid Bioch 1989; 32: 243.
- 18. Hurley DM, Accili D, Strakis CA, Karl M, Vamvakopoulos N, Rorer E, Constantine K, Taylor SI, Chrousos GP. Point mutation causing a single amino acid substitution in the hormone binding domain of the glucocortiocoid receptor in famillial glucocorticoid resistance. J Clin Invest 1991; 87: 680.
- 19. Brufsky AM, Malchoff DM, Javier EC, Reardon G, Rowe D, Malchoff CD. A glucocorticoid receptor mutation in a subject with primaery cortisol resistance. Trans Assoc Am Physicians 1990; 103: 53.
- 20. Lamberts SWJ, Koper JW, Biemond P, Denholder FH, Dejong FH: Cortisol Receptor Resistance - The variability of its clinical presentation and response to treatment. J Clin Endocrin Metab 1992; 74: 313.
- 21. Lane SJ, Lee TH. Glucocorticoid receptor characteristics in monocytes of patients with corticosteroid resistant bronchial asthma. Am Rev Respir Dis 1991; 143: 1020-1024.
- 22. Potocnik U, Ferkolj I, Glavac D, et al. Polymorphism in multidrug resistance 1 (MDR1) gene associated with refractory Crohn disease and ulcerative colitis. Genes Immun 2004; 5: 530-539.
- 23. Honda M, Orii F, Arabe T, et al. Expression of glucocorticoid receptor beta in lymphocytes of patients with glucocorticoid-resistance ulcerative colitis. Gastroenterology 2000; 118: 859-866.
- 24. De Iudicibus S, Stocco G, Martelossi S, et al. Association of BII polymorphism of the glucocorticoid receptor gene locus with response to glucocorticoids in inflammatory bowel disease. Gut 2007; 56: 1319-1320.
- 25. Matouš J. Úloha glukokortikoidů a kortikorezistence u idiopatických střevních zánětů. Čes a Slov Gastroent a Hepatol 2007; 61: 327-336.
- 26. Farrell RJ, Kelleher D. High multidrug resistance (P-glycoprotein 170) expression in inflammatory bowel disease patients who fail medical therapy. Gastroenterology 2000; 25: 111-122.
- 27. Flood L, Lofberg R, Syierna P, et al. Glucocorticoid receptor mRNA in patients with ulcerative colitis: a study of responders and nonrespoders to glucocorticosteroid therapy. Inflamm Bowel Dis 2001; 7: 202-209.
- 28. Bantel H, Domschke W, Schulze-Osthoff K, et al. Abnormal activation of transcription factor NF-.B involved in steroid resistance in chronic inflammatory bowel disease. Am J Gastroenterol 2000; 95: 1845-1846.
- 29. Modigliani R, Mary JY, Simon JF, Cortot A, Soule JC, Gendre JP, Rene E. Clinical, biological and endoscopic picture of attacks of Crohn’s disease. Evolution on prednisolone. Gastroenterology 1990; 98: 811-818.
- 30. Summers RW, Swith DM, Sessions JT, et al. National Cooperative Crohn’s Disease Study: results of drug treatment. Gastroenterology 1979; 77: 847-869.
- 31. Kjeldsen J. Treatment of ulcerative colitis with high dose of oral prednisolone. The rate of remission, the need for surgery, ant the effect of prolonging the treatment. Scan J Gastroent 1993; 28: 821-826.
- 32. Faubion WA Jr., Lotus EV Jr., Harmsen WS, et al. The natural history of corticosteroid therapy for inflammatory bowel disease: a population-based study. Gastroenterology 2001; 121: 255-260.
- 33. Creed TJ, Probert SJ. Revie artikle: steroid resistance in inflammatory bowel disease - mechanisms and therapeutic strategie. Aliment Pharmacol Ther 2007; 25: 111-122.
- 34. Leden P. Periferní metabolizmus glukokortikoidů: klinické aspekty. Čes a Slov Gastroenterol a Hepatol 2007; 61: 139-149.
- 35. Voderholzer U, Hohagen F, Postler E, Berger M, Bauer J. Zirkadiane Rhytmik von Zytokinen und Schlaf-Wach-Rytmus. Z Allg Med 1995; 71: 228-238.
Pro přístup k článku se, prosím, registrujte.
Výhody pro předplatitele
Výhody pro přihlášené